Cinetica
Definizione
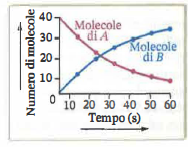
La termodinamica stabilisce se un processo chimico è favorito dal punto di vista energetico, ma non fornisce indicazioni sul ritmo con cui esso procede. La cinetica chimica, invece, analizza la velocità delle reazioni e mette in relazione le misure sperimentali con ipotesi sul meccanismo, ossia sulla sequenza di stadi elementari che conduce dai reagenti ai prodotti. Operativamente, la velocità di reazione si esprime come variazione della concentrazione di una specie nell’unità di tempo e può essere riferita tanto alla scomparsa dei reagenti quanto alla formazione dei prodotti. Un tracciato quantitativo dell’andamento temporale è mostrato in (Figura 04.08-01), dove il numero di molecole (o la concentrazione) è riportato in funzione del tempo.
Per una reazione generica con stechiometria \(\sum_i \nu_i \mathrm{A}_i \to \sum_j \nu_j' \mathrm{B}_j\), la velocità istantanea si può definire come:
\[ v(t) = -\,\frac{1}{\nu_i}\,\frac{\mathrm{d}[\mathrm{A}_i]}{\mathrm{d}t} = \frac{1}{\nu_j'}\,\frac{\mathrm{d}[\mathrm{B}_j]}{\mathrm{d}t}, \] dove \(\nu_i\) e \(\nu_j'\) sono i coefficienti stechiometrici positivi delle specie consumate e formate, rispettivamente.
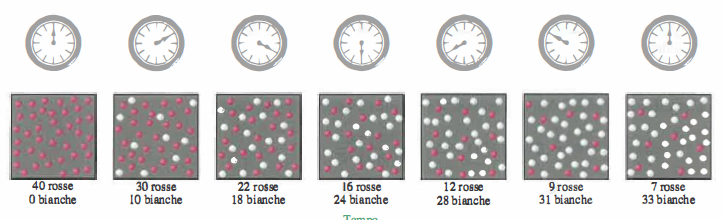
La conoscenza delle velocità è cruciale in molti ambiti applicativi: la crescita dello strato di ossidi in un processo di corrosione, la reticolazione di una resina epossidica in un composito, la degradazione fotochimica di un colorante in un impianto di trattamento delle acque, o la cinetica di assorbimento e trasformazione di un principio attivo in un sistema di rilascio controllato. La (Figura 04.08-02) schematizza un modo utile di visualizzare, a livello molecolare, gli eventi cinetici che intercorrono tra urti, formazione di stati intermedi e comparsa dei prodotti. In molte reazioni è possibile seguire la velocità per via spettrofotometrica osservando variazioni di assorbanza o di colore nel tempo, come esemplificato in (Figura 04.08-03).
Si consideri la reazione esotermica di combustione del metano:
CH4(g) + 2 O2(g) → CO2(g) + 2 H2O(g) + 211 kcal
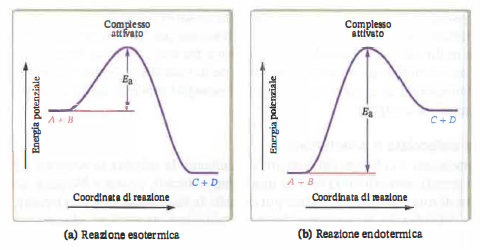
Perché la trasformazione abbia luogo, i legami C–H e O–O devono rompersi e nuovi legami C–O e O–H devono formarsi. L’energia necessaria alla rottura dei legami preesistenti proviene dagli urti tra particelle; solo una parte degli urti, quelli sufficientemente energetici e con orientazione adeguata, sono “efficaci” e portano a prodotti. La minima energia che le specie reagenti devono acquisire per intraprendere il percorso reattivo è l’energia di attivazione, \(E_a\). L’andamento dell’energia potenziale lungo la coordinata di reazione è illustrato in (Figura 04.08-04) per casi esotermici ed endotermici:
- La trasformazione procede attraverso uno stato di transizione, o complesso attivato, estremamente fugace e non isolabile, in cui si osserva la riorganizzazione simultanea dei legami; la sua natura effimera discende dall’instabilità intrinseca e dalla posizione al vertice della barriera energetica;
- La differenza tra l’energia del complesso attivato e quella dei reagenti definisce \(E_a\); aumentando la temperatura, la distribuzione di Maxwell–Boltzmann sposta verso energie maggiori la frazione di molecole, incrementando il numero di urti capaci di superare la barriera e, quindi, la velocità di reazione;
- L’andamento empirico della costante cinetica con la temperatura è descritto dall’equazione di Arrhenius: \[ k = A\, e^{-\tfrac{E_a}{RT}} \] dove \(k\) è la costante cinetica, \(R\) la costante dei gas, \(T\) la temperatura assoluta, \(A\) il fattore pre-esponenziale correlato alla frequenza di collisione e ai requisiti sterici;
- Nel caso esotermico mostrato in (Figura 04.08-04), l’energia dei prodotti è inferiore a quella dei reagenti e il bilancio energetico è negativo; la barriera in direzione diretta è inferiore a quella della reazione inversa di un ammontare pari a \(|\Delta E|\).
Per una reazione endotermica, ad esempio la decomposizione elettrolitica dell’acqua:
energia + 2 H2O(l) → 2 H2(g) + O2(g)
il profilo energetico in (Figura 04.08-04) evidenzia una barriera elevata: l’elevato \(E_a\) rende trascurabile la frazione di urti efficaci a temperatura ambiente, spiegando la lentezza della reazione in assenza di apporto energetico e catalizzatori.
Due considerazioni operative completano il quadro. Primo, l’orientazione delle molecole agli urti contribuisce al fattore \(A\): anche urti energeticamente idonei possono non essere efficaci se la geometria non consente la formazione del complesso attivato. Secondo, dalla forma lineare della relazione di Arrhenius, \(\ln k = \ln A - E_a/(RT)\), un grafico di \(\ln k\) in funzione di \(1/T\) consente di stimare \(E_a\) dalla pendenza, fornendo un metodo sperimentale robusto per caratterizzare le barriere energetiche dei processi reattivi.
Diversi aspetti incidono in modo decisivo sull’andamento temporale di una trasformazione chimica. Tra i più rilevanti si annoverano:
- struttura elettronica e natura dei reagenti;
- geometria, ingombro sterico e orientamento nelle collisioni molecolari;
- concentrazione dei reagenti o, per i gas, pressione parziale;
- temperatura del sistema reagente;
- fase fisica e grado di dispersione delle specie coinvolte;
- presenza di sostanze catalitiche, omogenee o eterogenee.
Struttura dei reagenti
La natura dei legami e la distribuzione elettronica nei reagenti condizionano l’energia necessaria per avviare la trasformazione. Reazioni fra ioni in soluzione, dove i reticoli ionici risultano già dissociati, tendono a essere rapide perché la barriera energetica di accesso allo stato di transizione è contenuta. All’opposto, processi che esigono la rottura di legami covalenti forti sono più lenti, poiché la fase iniziale di scissione richiede un’energia di attivazione più elevata. Le energie di dissociazione di legame, gli effetti induttivi e di risonanza, nonché l’eventuale stabilizzazione degli stati di transizione, contribuiscono alla determinazione di \(E_{\mathrm{a}}\) e, di conseguenza, alla velocità. In ambito organico, ad esempio, substrati con gruppi elettron-attrattori possono accelerare meccanismi elettrofili, mentre sostituenti voluminosi possono penalizzare meccanismi concertati che richiedono approcci stericamente esigenti.
Geometria molecolare e orientamento
Dimensioni e forma influenzano la probabilità che due particelle si urtino con l’assetto spaziale corretto per dare prodotti. L’ingombro sterico di gruppi voluminosi può schermare il sito reattivo, diminuendo la frazione di collisioni efficaci. Nella teoria delle collisioni questo effetto è ricompreso nel cosiddetto fattore sterico \(P\), che modula la frequenza di urti produttivi. In sintesi: non basta che le particelle dispongano dell’energia sufficiente; è imprescindibile che l’orientazione relativa soddisfi i requisiti geometrici dello stato di transizione.
Concentrazione dei reagenti
A parità di altre condizioni, una maggiore concentrazione accresce la frequenza di collisione per unità di volume e tempo, aumentando la probabilità di urti efficaci. In fase gassosa, un analogo ragionamento si applica alle pressioni parziali. Per reazioni eterogenee, oltre alla concentrazione contano la disponibilità di siti attivi e i processi di trasporto verso l’interfaccia. Un esempio semplice è l’azione dell’acido cloridrico su magnesio metallico: soluzioni più concentrate di HCl forniscono idrogeno più rapidamente, a parità di temperatura e superficie del metallo esposta.
Temperatura dei reagenti
L’aumento di temperatura eleva l’energia cinetica media delle particelle e la frazione di molecole con energia superiore alla barriera di attivazione. La dipendenza della costante cinetica \(k\) dalla temperatura è descritta, per molte reazioni, dall’equazione di Arrhenius: \(k = A e^{-E_{\mathrm{a}}/(RT)}\). Una variazione moderata di temperatura può produrre effetti marcati sulla velocità: per esempio, passando da 293 K a 303 K, una reazione con \(E_{\mathrm{a}} \approx 50\,\mathrm{kJ\,mol^{-1}}\) mostra un incremento di velocità di circa un fattore 2, in accordo con la distribuzione di Maxwell-Boltzmann delle energie.
Fase fisica dei reagenti
La reattività dipende anche dallo stato di aggregazione. In fase solida la mobilità dei costituenti è limitata e la reazione spesso procede alla superficie o lungo difetti del reticolo; la velocità può aumentare in modo significativo riducendo la dimensione delle particelle, così da incrementare l’area specifica. In fase liquida e gassosa, la maggiore libertà di moto e la più agevole miscelazione favoriscono collisioni frequenti e quindi velocità più elevate. Nei sistemi eterogenei, fenomeni diffusivi e di adsorbimento ai siti attivi possono divenire stadi limitanti.
Impiego di un catalizzatore
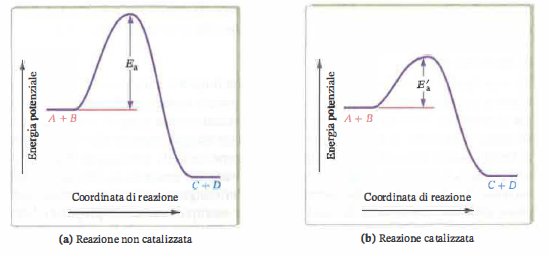
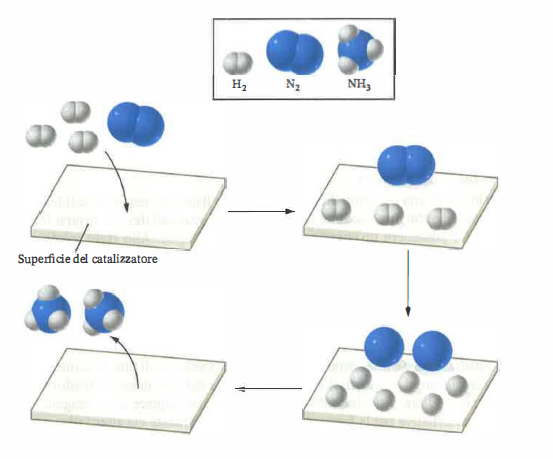
Un catalizzatore accelera la reazione proponendo un percorso alternativo con energia di attivazione inferiore, senza modificare il bilancio stechiometrico complessivo e risultando invariato al termine del ciclo catalitico. L’effetto è rappresentato schematicamente nella (Figura 04.08-05). Si distinguono catalizzatori omogenei (stessa fase) ed eterogenei (fase diversa), ciascuno con proprie caratteristiche di attività e selettività. Applicazioni industriali includono, tra le molte, l’ossidazione di CO nei convertitori catalitici automobilistici su metalli del gruppo del platino e la sintesi dell’ammoniaca, dove solidi a base di ferro promossi facilitano la dissociazione dell’azoto molecolare; un modello molecolare dell’azione del catalizzatore solido nella sintesi dell’ammoniaca è illustrato nella (Figura 04.08-06). In ambito biologico, gli enzimi svolgono il ruolo di catalizzatori altamente specifici, con elevata efficienza (turnover), come nel caso della catalasi che accelera la decomposizione del perossido di idrogeno.
Consideriamo la decomposizione termica in fase gassosa del pentossido di diazoto, \(\mathrm{N_2O_5}\), che produce diossido di azoto e ossigeno molecolare secondo:
\[ 2\,\mathrm{N_2O_5}(g) \;\longrightarrow\; 4\,\mathrm{NO_2}(g) + \mathrm{O_2}(g) \]
La velocità può essere espressa in funzione della variazione temporale delle concentrazioni, tenendo conto dei coefficienti stechiometrici:
\[ v \;=\; -\frac{1}{2}\,\frac{d[\mathrm{N_2O_5}]}{dt} \;=\; \frac{1}{4}\,\frac{d[\mathrm{NO_2}]}{dt} \;=\; \frac{d[\mathrm{O_2}]}{dt} \]
Mantenendo costanti natura chimica, temperatura, stato fisico e assenza/presenza di catalizzatore, la velocità sperimentale risulta proporzionale a una potenza della concentrazione dei reagenti. Per \(\mathrm{N_2O_5}\) si osserva:
\[ v \;\propto\; [\mathrm{N_2O_5}]^n \]
dove l’esponente \(n\), determinato sperimentalmente, è l’ordine della reazione rispetto al reagente considerato. Introducendo la costante cinetica \(k\), si ottiene l’equazione cinetica:
\[ v \;=\; k\, [\mathrm{N_2O_5}]^n \]
Per questa decomposizione si trova \(n = 1\); la legge cinetica è quindi del primo ordine: \(v = k\, [\mathrm{N_2O_5}]\).
In termini generali, per una trasformazione del tipo:
\[ A \;\longrightarrow\; \text{prodotti} \]
la legge di velocità assume la forma:
\[ v \;=\; k\,[A]^n \]
Per una reazione bimolecolare:
\[ A + B \;\longrightarrow\; \text{prodotti} \]
si utilizza in genere:
\[ v \;=\; k\,[A]^n [B]^{n'} \]
L’ordine rispetto ad A è \(n\), quello rispetto a B è \(n'\), e l’ordine globale è \(n + n'\). Questi esponenti, così come il valore di \(k\) (le cui unità dipendono dall’ordine complessivo), si ottengono da misure cinetiche e non sono deducibili in modo affidabile dalla sola stechiometria. Non è infrequente riscontrare ordini frazionari, zero o, in presenza di inibizioni, anche negativi. In condizioni di grande eccesso di un reagente, una legge del secondo ordine può ridursi a un comportamento pseudo-primo ordine, con utili semplificazioni sperimentali.
La conoscenza quantitativa della legge di velocità e di \(k\) permette di definire le condizioni operative per massimizzare la produttività e individuare gli stadi lenti che governano la durata complessiva dei processi.
L’equazione globale bilanciata sintetizza reagenti e prodotti, ma non descrive necessariamente la sequenza degli eventi microscopici. Spesso la trasformazione procede attraverso una serie di stadi elementari, ciascuno con propria stechiometria e propria legge di velocità. La successione ordinata di tali passaggi costituisce il meccanismo di reazione.
Un caso classico è la formazione di \(\mathrm{NO_2}\) a partire da ossido di azoto e ossigeno:
\[ 2\,\mathrm{NO}(g) + \mathrm{O_2}(g) \;\longrightarrow\; 2\,\mathrm{NO_2}(g) \]
Le evidenze sperimentali indicano che la reazione non avviene tramite una singola collisione di tre particelle, bensì mediante due stadi elementari che coinvolgono l’intermedio \(\mathrm{N_2O_2}\):
\(\mathrm{2\,NO}(g) \;\xrightarrow{\;\text{stadio 1}\;}\; \mathrm{N_2O_2}(g)\)
\(\mathrm{N_2O_2}(g) + \mathrm{O_2}(g) \;\xrightarrow{\;\text{stadio 2}\;}\; 2\,\mathrm{NO_2}(g)\)
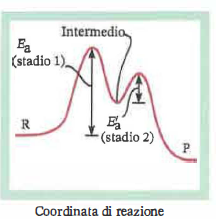
\(\mathrm{N_2O_2}\) è un intermedio di reazione: compare nel meccanismo ma non nella somma globale, e può trovarsi in un minimo locale dell’energia potenziale. Diversamente, lo stato di transizione, associato al massimo di energia lungo la coordinata di reazione, non è isolabile. La (Figura 04.08-07) schematizza un profilo energetico con due massimi, corrispondenti agli stadi elementari.
Per gli stadi elementari, l’ordine di reazione coincide con i coefficienti stechiometrici dello stadio stesso, poiché riflette la sua molecolarità. Nel caso considerato:
\[ v_1 \;=\; k_1\,[\mathrm{NO}]^{2} \]
\[ v_2 \;=\; k_2\,[\mathrm{N_2O_2}]\,[\mathrm{O_2}] \]
Quando più stadi si susseguono, lo stadio più lento (determinante la velocità) controlla l’andamento della reazione complessiva; è su di esso che agiscono in modo più incisivo modifiche di temperatura, concentrazione o catalisi. Molti meccanismi della chimica organica prevedono catene di passaggi con intermedi reattivi (carbocationi, radicali, carbanioni) e possono includere equilibri preesistenti o approssimazioni di stato stazionario per derivare le leggi di velocità osservate sperimentalmente.