Isomeri conformazionali (conformeri) negli alcani e nei cicloalcani
Definizione
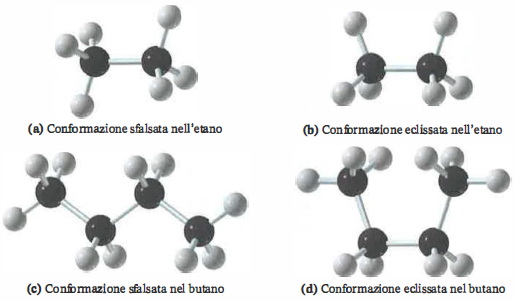
La rotazione attorno a un legame singolo carbonio–carbonio, di natura σ, è intrinsecamente agevole e consente a una stessa molecola di assumere una molteplicità di disposizioni spaziali, come nel caso dell’etano, che generano un continuum di forme osservabili, cfr. (Figura 06.04-01) e (Figura 06.04-01). Tali forme, interconvertibili per rotazione intorno ai legami C–C e in rapido equilibrio a temperatura ambiente, sono chiamate conformazioni, conformeri o isomeri conformazionali. L’energia potenziale associata alla rotazione varia periodicamente con l’angolo diedro \(\phi\) e, per sistemi semplici come l’etano, può essere efficacemente descritta da una funzione del tipo
\[ V(\phi) = \tfrac{V_3}{2}\,\bigl(1 - \cos 3\phi\bigr) \]
dove i minimi (conformazione sfalsata) e i massimi (conformazione eclissata) si alternano ogni 60°. La barriera torsionale dell’etano è dell’ordine di poche kcal/mol (circa 2,9 kcal/mol), sufficiente a definire stati preferiti ma troppo bassa per consentire l’isolamento dei conformeri in condizioni ordinarie.
Negli alcani più complessi, la varietà conformazionale cresce con il numero di legami C–C. Nella molecola di butano, rappresentabile con proiezioni di Newman lungo il legame C2–C3, si individuano conformeri “limite” riportati in (Figura 06.04-01) e (Figura 06.04-01), tra i quali esiste una famiglia continua di conformazioni intermedie generate da rotazioni successive. A temperatura ambiente i conformeri sono separati da barriere energetiche modeste (dell’ordine di 3–6 kcal/mol), e si interconvertono rapidamente.
Dal punto di vista energetico, risultano più favoriti i conformeri sfalsati per minimizzazione della repulsione elettronica tra legami vicini (minore tensione torsionale). Nel butano, fra i conformeri sfalsati, si distinguono:
- conformazione anti, in cui i due gruppi metilici sono disposti a 180°: è la più stabile per minimi ingombri sterici;
- conformazione gauche, con i metili separati da 60°: presenta un lieve incremento energetico per interazione sterica residua, tipicamente di circa 0,8–1,0 kcal/mol rispetto all’anti.
La popolazione relativa dei conformeri è regolata dalla relazione di Boltzmann, \(N_i \propto e^{-E_i/RT}\), che privilegia i minimi di energia potenziale. Le conformazioni eclissate, caratterizzate da massima sovrapposizione dei legami e da maggiori repulsioni, rappresentano i massimi del profilo energetico e risultano scarsamente popolate.
Le principali componenti che determinano la stabilità conformazionale degli alcani includono:
- tensione torsionale, dovuta all’allineamento eclissato di legami e alla repulsione tra coppie di elettroni di legame;
- interazioni steriche (ingombro), rilevanti quando gruppi voluminosi si avvicinano oltre la distanza di Van der Waals;
- eventuali contributi iperconiugativi, che stabilizzano le conformazioni sfalsate per migliore sovrapposizione di orbitali σ.
I cicloalcani manifestano ricchezza conformazionale, con l’eccezione del ciclopropano, costretto alla planarità per la dimensione minima dell’anello e soggetto a elevata tensione angolare. Per cicli più ampi, la non planarità riduce sia la tensione angolare sia la tensione torsionale: il ciclobutano adotta una forma leggermente “piegata” per diminuire l’eclissamento, mentre il ciclopentano preferisce conformazioni a “busta” o “mezza torsione”.
Gli anelli a sei termini, di particolare rilevanza in chimica biologica e dei materiali (ad esempio in carboidrati come il glucosio), presentano una conformazione a energia minima detta “a sedia”. In tale assetto:
- gli angoli di legame C–C si avvicinano a 109,5°, in linea con la geometria tetraedrica dell’atomo di carbonio ibridizzato sp³;
- tutti i legami adiacenti risultano sfalsati, con riduzione della tensione torsionale;
- le distanze tra sostituenti sono massimizzate, contenendo le repulsioni steriche.
Conformazioni alternative includono la “barca”, più elevata in energia per eclissamenti diffusi e per le repulsioni tra i cosiddetti atomi “pennone” (flagpole), e la “barca contorta” (twist-boat), leggermente più stabile della barca ma sempre meno favorevole della sedia. La conversione sedia–sedia (ring flip) supera una barriera di circa 10,0–11,0 kcal/mol, consentendo a temperatura ambiente una rapida interconversione che scambia le posizioni degli atomi e dei sostituenti tra siti assiali ed equatoriali.
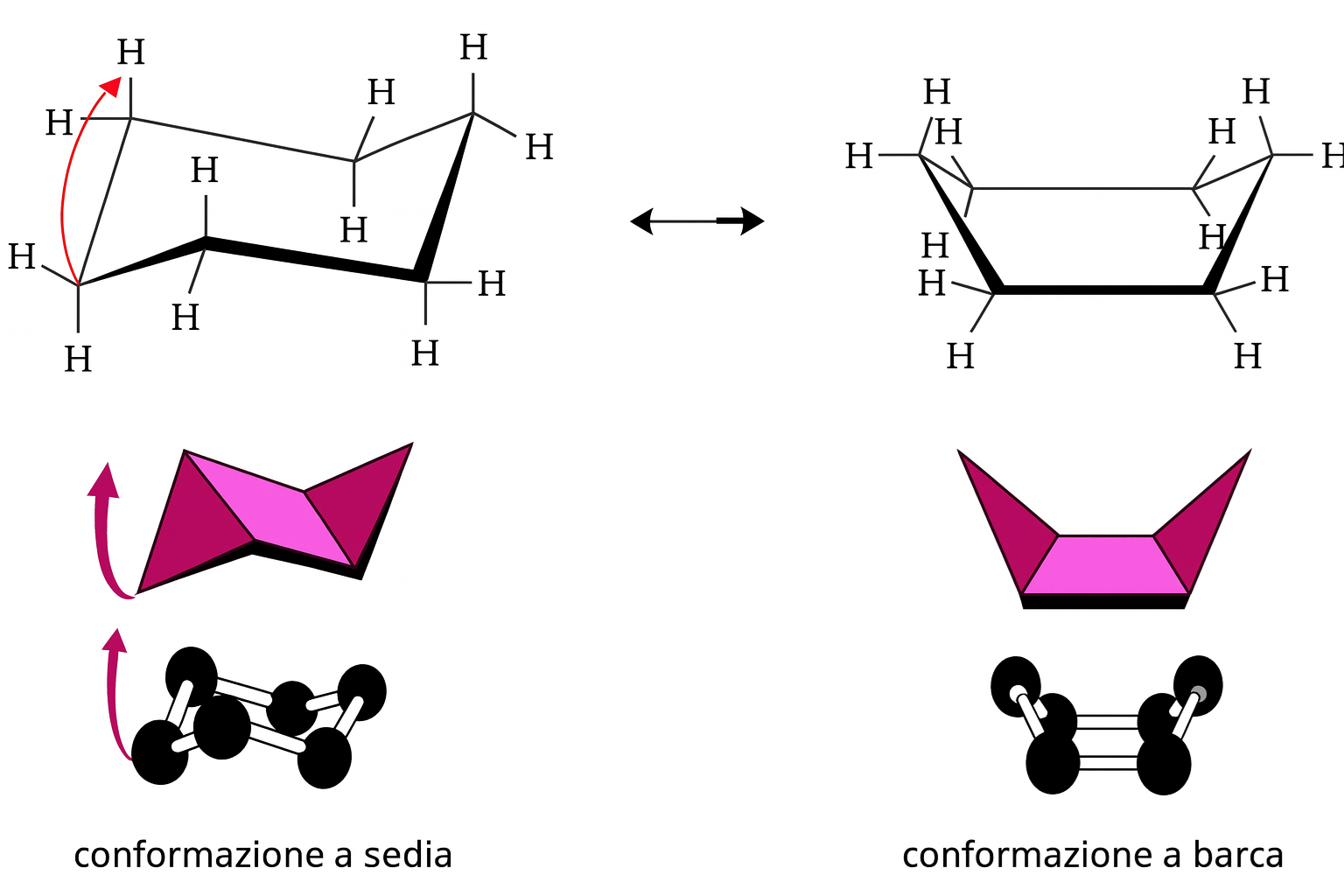 |
| Conformazioni del cicloesano. |
Nel cicloesano, i legami C–H (o C–R) si classificano in base all’orientamento rispetto all’asse dell’anello:
- assiali (A), orientati alternativamente sopra e sotto il piano medio dell’anello;
- equatoriali (E), disposti approssimativamente lungo la circonferenza dell’anello, cioè quasi nel suo piano medio.
La preferenza conformazionale dei sostituenti verso siti equatoriali è spesso marcata, poiché l’occupazione di posizioni assiali introduce interazioni 1,3-diaxiali con i sostituenti assiali del medesimo lato dell’anello, aumentando l’energia del sistema. Nella sedia ideale, la collocazione equatoriale minimizza tali interazioni steriche e massimizza la stabilità.
 |
| Sostituenti assiali ed equatoriali nel cicloesano. |