Isomeria geometrica: conseguenza
Definizione
Nei cicloalcani la libera rotazione attorno al legame semplice C–C è vincolata dalla chiusura dell’anello: la conformazione non può variare senza alterare la geometria del ciclo e, di conseguenza, si osserva isomeria geometrica di tipo cis-trans a seconda che due sostituenti si trovino dal medesimo lato (cis) oppure da lati opposti (trans) rispetto al piano medio dell’anello.
Un analogo impedimento si manifesta negli alcheni. Il doppio legame C=C comprende un legame σ e un legame π; la rotazione attorno all’asse del doppio legame richiederebbe la rottura del legame π, con una barriera energetica molto elevata. Indicativamente, l’energia termica disponibile a temperatura ambiente è dell’ordine di \(RT \approx 2,5\,\mathrm{kJ\,mol^{-1}}\), mentre l’energia associata alla rottura del legame \(\pi\) è dell’ordine di \(E_{\pi} \approx 250\,\mathrm{kJ\,mol^{-1}}\): ne consegue che la rotazione è, di fatto, preclusa nelle condizioni ordinarie.
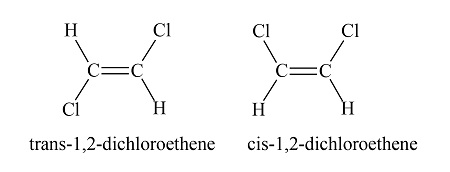
Per un doppio legame C=C, l’isomeria geometrica è possibile quando ciascuno dei due atomi di carbonio sp\(^2\) è legato a due gruppi non identici. In tale circostanza, se i sostituenti di riferimento risultano dalla stessa parte del piano del doppio legame si ottiene l’isomero cis, se si collocano da parti opposte si ottiene l’isomero trans. Si considerino i due isomeri del 1,2-dicloroetene, in cui ciascun carbonio vinilico porta un atomo di H e un atomo di Cl:
 |
| Isomeria cis-trans negli alcheni. |
Nella struttura a sinistra i due atomi di cloro sono collocati dallo stesso lato del doppio legame: l’isomero è quindi cis e si denomina cis-1,2-dicloroetene. Nella struttura a destra i clori risultano su lati opposti: l’isomero è trans, ovvero trans-1,2-dicloroetene. Se, invece, uno dei due carboni della doppia lega due sostituenti identici, la distinzione cis-trans non è definibile. Ciò avviene, ad esempio, nel 1,1-dicloroetene:
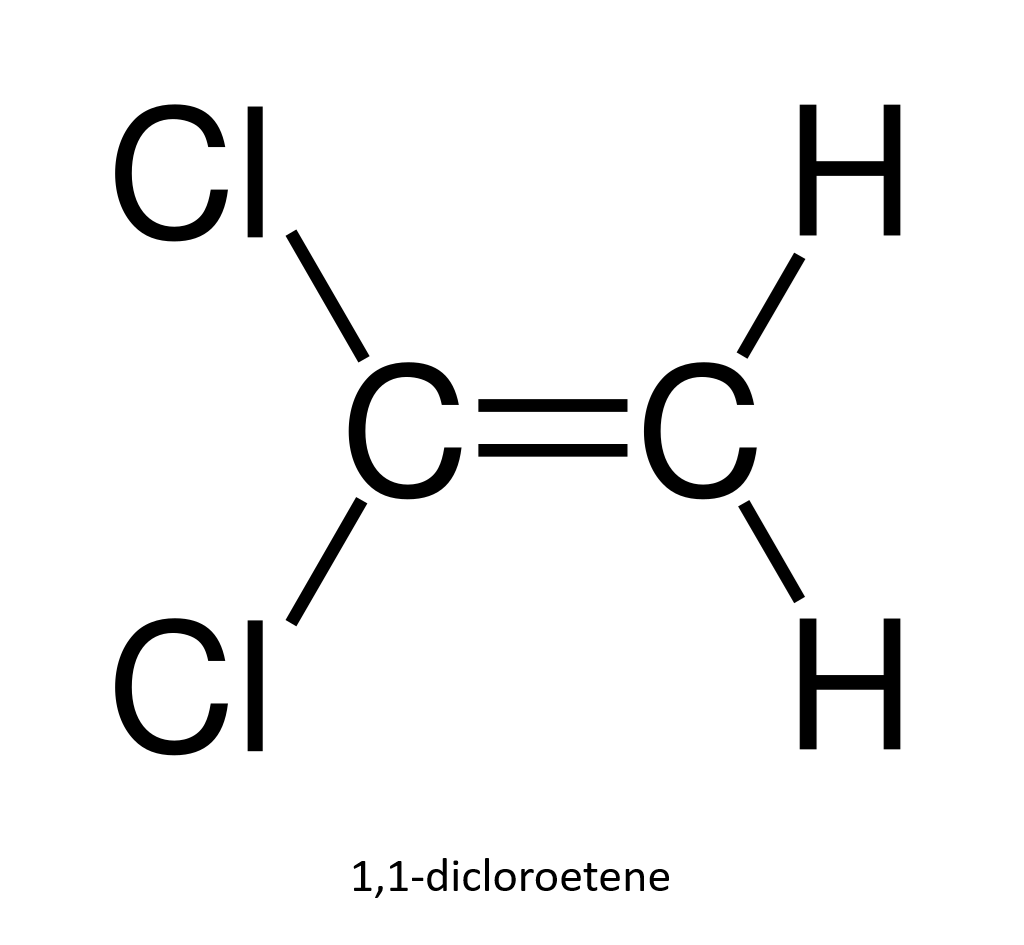 |
| Isomeria E/Z negli alcheni. |
In generale, il criterio cis-trans è immediato per alcheni disostituiti. Per alcheni tri- o tetrasostituiti, oppure quando l’assegnazione “due uguali dallo stesso lato” non è applicabile, è preferibile adottare la nomenclatura E/Z basata sulle priorità CIP.
Criteri E/Z e priorità CIP
Il sistema E/Z estende il concetto di isomeria geometrica a doppi legami con sostituzione complessa, seguendo le regole di Cahn–Ingold–Prelog (CIP). La procedura è la seguente:
- su ciascun carbonio del doppio legame si attribuisce la priorità ai due sostituenti in base al numero atomico del primo punto di differenza lungo la catena; il sostituente con numero atomico maggiore ha priorità superiore;
- in caso di parità, si procede lungo i sostituenti finché non si trova una differenza; si applicano le regole per gestire ramificazioni e legami multipli;
- se i due sostituenti a priorità più alta si trovano dallo stesso lato del doppio legame, la configurazione è Z (zusammen);
- se risultano su lati opposti, la configurazione è E (entgegen).
Nel 1,2-dicloroetene, Cl ha priorità maggiore rispetto a H; l’isomero con i due Cl dallo stesso lato è Z e coincide con il cis, mentre quello con i Cl opposti è E e coincide con il trans. Un esempio ulteriore, didatticamente equivalente ma diverso, è il 2-butene: i due metili dalla stessa parte conferiscono la forma cis (Z), da lati opposti la forma trans (E).
Acidi grassi insaturi: forma cis vs trans e conseguenze
Gli acidi grassi sono acidi carbossilici a catena lunga; quelli di origine vegetale sono spesso insaturi, mentre nei grassi animali prevalgono le catene sature. L’acido oleico:
 |
| Idratazione elettrofila degli alcheni. |
è il principale componente dell’olio d’oliva. Il nome IUPAC, acido cis-9-ottadecenoico, indica che il doppio legame in posizione 9 presenta configurazione cis:
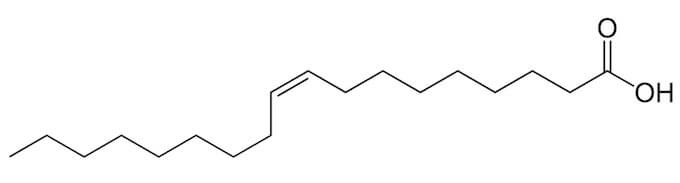 |
| Acido grasso insaturo. |
La configurazione cis induce un “gomito” nella catena idrocarburica, conferendo rigidità locale e una traiettoria piegata. L’isomero geometrico trans-9-ottadecenoico (acido elaidico), presente in natura solo in tracce, possiede invece una catena pressoché rettilinea e rigida:
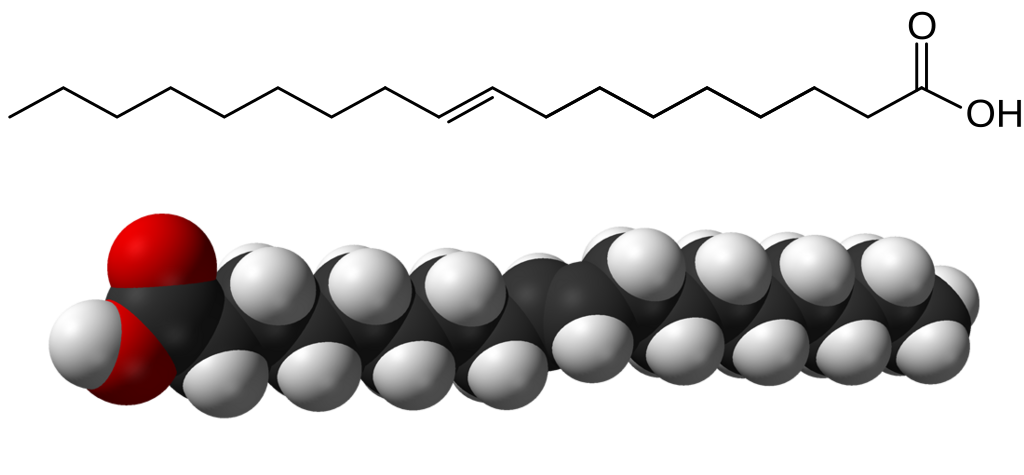 |
| Modello molecolare di acido grasso. |
Le diverse geometrie hanno ricadute sulle proprietà fisiche e biologiche:
- impaccamento solido: le catene trans, quasi lineari, si dispongono più densamente, innalzando il punto di fusione rispetto alle corrispondenti cis;
- fluidità: le catene cis, con flessione al doppio legame, riducono le interazioni di van der Waals e favoriscono la fluidità di oli e membrane;
- stabilità conformazionale: la rotazione è inibita al doppio legame in entrambe le configurazioni, ma la distribuzione conformazionale lungo la catena differisce per l’angolo imposto alla regione insatura.
La maggior parte degli acidi grassi trans introdotti con gli alimenti deriva da processi tecnologici, in particolare dall’idrogenazione parziale di oli vegetali, durante i quali può avvenire isomerizzazione catalitica da cis a trans. Evidenze consolidate indicano che l’assunzione di acidi grassi trans di origine industriale aumenta il colesterolo LDL e riduce l’HDL, con incremento del rischio cardiovascolare; ulteriori studi hanno messo in relazione tali isomeri con un aumento del rischio di diabete di tipo 2. Le raccomandazioni di organismi internazionali (ad esempio OMS ed EFSA) promuovono la riduzione dell’apporto di acidi grassi trans nella dieta.








