Alcheni e e proprietà fisiche alchini: strutture
Definizione
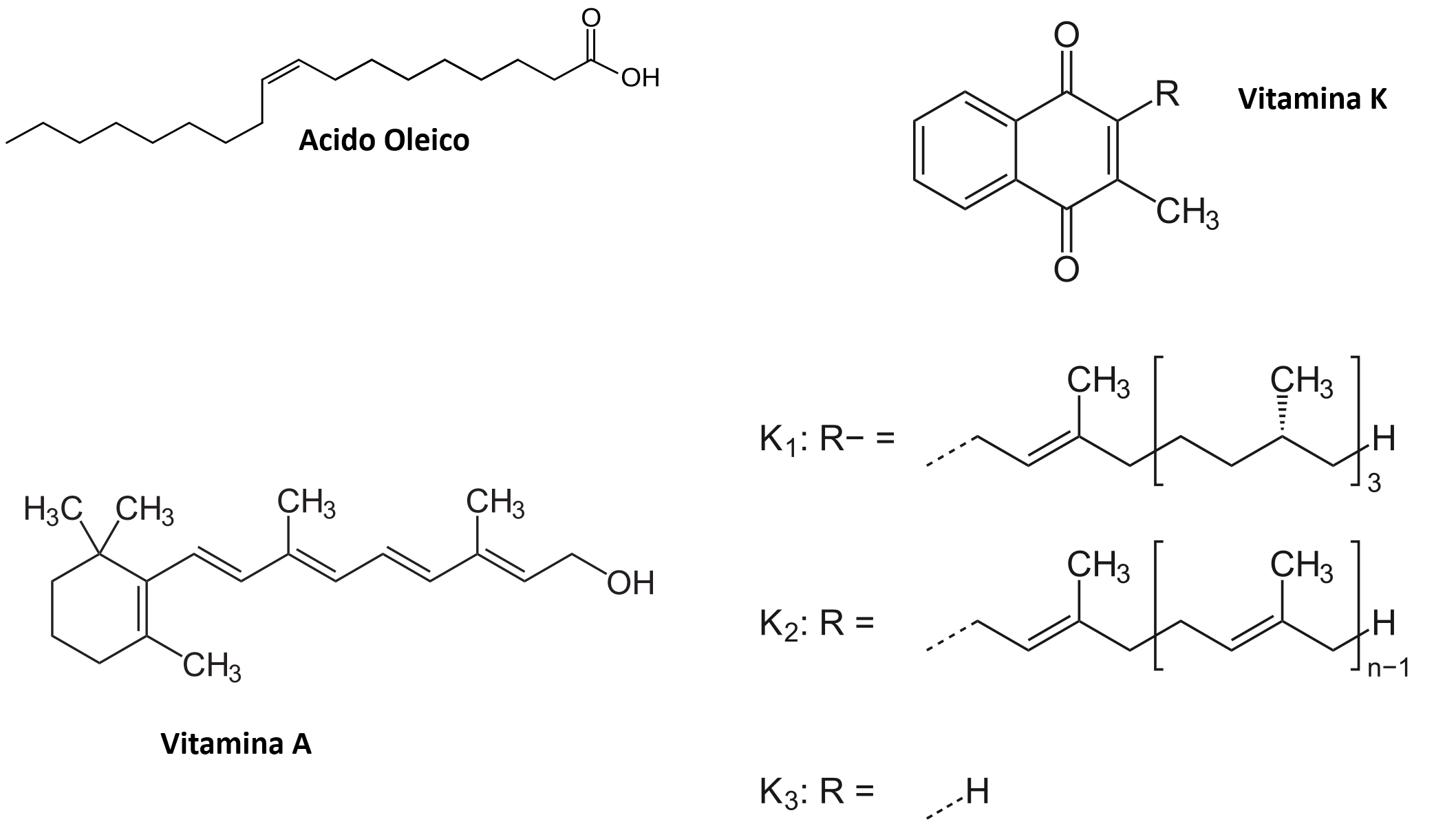
Una vasta gamma di molecole di interesse biologico, sia a catena aperta sia cicliche, deve le proprie proprietà alla presenza di doppi legami o di più doppi legami in coniugazione (Figura 06.06-01). Tra gli esempi più rilevanti si annoverano: acidi grassi monoinsaturi (un solo doppio legame), acidi grassi polinsaturi (due o più doppi legami), il retinal, componente della vitamina A fondamentale per la visione e dotato di una catena idrocarburica con 5 doppi legami coniugati, e la vitamina K, che include una porzione aromatica. Alcheni e alchini appartengono alla famiglia degli idrocarburi insaturi: gli alcheni sono caratterizzati dal gruppo funzionale carbonio–carbonio a doppio legame (C=C), mentre gli alchini presentano un triplo legame carbonio–carbonio (C≡C).
Per gli idrocarburi aciclici non ramificati, le relazioni stechiometriche di riferimento sono: alcani \( \mathrm{C_nH_{2n+2}} \), alcheni \( \mathrm{C_nH_{2n}} \), alchini \( \mathrm{C_nH_{2n-2}} \). In altre parole, a parità di numero di atomi di carbonio, un alchene possiede due idrogeni in meno rispetto all’alcano corrispondente, e un alchino due idrogeni in meno rispetto all’alchene correlato. Tali formule generali subiscono modifiche in presenza di cicli, sostituzioni o funzionalità addizionali.
| Classe | Formula generale | Struttura (esempio) | Denominazione (IUPAC / comune) | Formula molecolare | Formula condensata |
| Alcani | CnH2n+2 | H3C–CH3 | Etano (etano) | C2H6 | CH3–CH3 |
| H3C–CH2–CH3 | Propano | C3H8 | CH3–CH2–CH3 | ||
| H3C–CH2–CH2–CH3 | Butano | C4H10 | CH3–CH2–CH2–CH3 | ||
| Alcheni | CnH2n | H2C=CH2 | Etene (etilene) | C2H4 | CH2=CH2 |
| H2C=CH–CH3 | Propene | C3H6 | CH2=CH–CH3 | ||
| CH3–CH2–CH=CH2 | But-1-ene | C4H8 | CH3–CH2–CH=CH2 | ||
| Alchini | CnH2n−2 | HC≡CH | Etino (acetilene) | C2H2 | HC≡CH |
| HC≡C–CH3 | Propino | C3H4 | HC≡C–CH3 | ||
| CH3–CH2–C≡CH | But-1-ino | C4H6 | CH3–CH2–C≡CH |
La presenza dell’insaturazione determina un’ibridizzazione specifica degli atomi di carbonio coinvolti e la geometria locale. Nel doppio legame C=C ciascun carbonio è ibridizzato sp2 e forma tre legami σ disposti in un piano con angoli prossimi a 120°, mentre il legame π, generato dalla sovrapposizione laterale degli orbitali p non ibridi, è perpendicolare al piano σ. Nel triplo legame C≡C entrambi i carboni sono ibridizzati sp, con una disposizione lineare e angoli di 180°; il triplo legame comprende un legame σ e due legami π mutuamente perpendicolari. Nel confronto con il legame semplice C–C, le distanze medie sono: C–C ≈ 1,54 Å, C=C ≈ 1,34 Å, C≡C ≈ 1,20 Å, in accordo con l’aumentare dell’ordine di legame e dell’energia di legame.
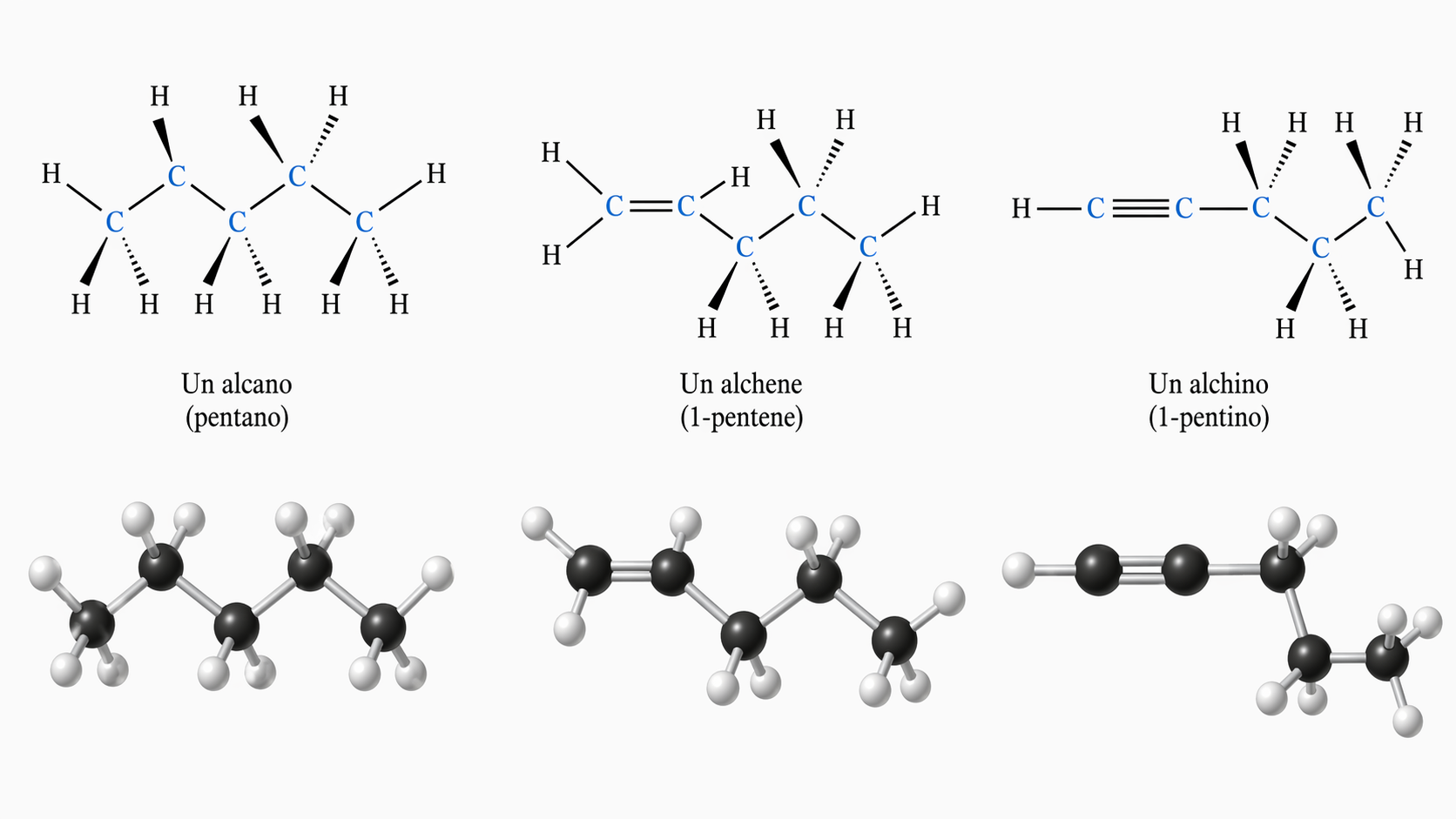
La rotazione intorno a C=C è inibita dalla componente π, con la conseguente possibilità di isomeria geometrica; viceversa, la linearità della porzione C≡C vincola l’orientazione dei sostituenti. Esempi rappresentativi di alcani, alcheni e alchini sono mostrati nella (Figura 06.06-02).
Alcani, alcheni, alchini e composti aromatici sono complessivamente poco polari: dominano le interazioni di dispersione di London, che aumentano al crescere della superficie molecolare e della polarizzabilità. Ne consegue che, a parità di altri fattori, l’allungamento della catena idrocarburica provoca un incremento delle temperature di fusione ed ebollizione, come sintetizzato nella (Tabella 06.06-01). La ramificazione, riducendo la superficie di contatto, tende invece ad abbassare il punto di ebollizione. Gli alcheni presentano spesso punti di ebollizione lievemente inferiori agli alcani isomerici, mentre gli alchini hanno valori confrontabili o leggermente più elevati quando la massa molecolare è simile, in funzione della forma e dell’impaccamento cristallino:
- Densità: gli idrocarburi leggeri sono meno densi dell’acqua, con valori tipici nell’intervallo 0,6–0,8 g·cm−3 a 20 °C;
- Solubilità: l’assenza di momenti dipolari marcati rende gli idrocarburi praticamente immiscibili in acqua, mentre risultano ben solubili in solventi a bassa polarità (es. esano, toluene), in accordo al principio di affinità tra soluto e solvente;
- Volatilità: diminuisce con l’aumento del numero di atomi di carbonio e con la riduzione della ramificazione, coerentemente con l’intensità delle forze di dispersione;
- Reattività e natura dell’insaturazione: il doppio legame comporta una regione elettronica ricca suscettibile ad addizioni elettrofile; il triplo legame, più corto e rigido, è ancora più ricco in densità elettronica π e conferisce agli alchini terminali un’acidità significativamente superiore a quella di alcani e alcheni (pKa intorno a 25), per effetto dell’ibridizzazione sp.
In sintesi, la natura dell’insaturazione C=C o C≡C influenza simultaneamente geometria, proprietà fisiche e reattività: la planarità sp2 e la linearità sp determinano i valori caratteristici degli angoli di legame (circa 120° e 180° rispettivamente), mentre le deboli interazioni intermolecolari spiegano i bassi punti di fusione ed ebollizione, la bassa densità e la scarsa solubilità in mezzi acquosi tipiche degli idrocarburi.
 |
| Alcani, alcheni e alchini. |
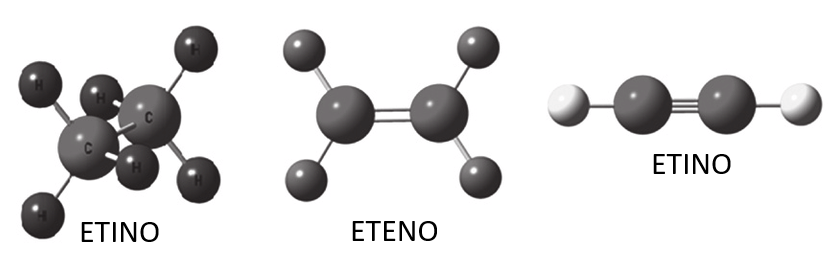 |
| Modelli molecolari di alcano, alchene e alchino. |
Caratteristiche fisiche di alcheni e alchini
| Nome | Formula molecolare | Formula di struttura | T. di fusione (°C) | T. di ebollizione (°C) | Nota |
|---|---|---|---|---|---|
| Etene | C₂H₄ | CH₂=CH₂ | −169.1 | −103.7 | Gas utilizzato in passato come anestetico (etilene), oggi studiato in tossicologia ambientale. |
| Propene | C₃H₆ | CH₂=CH–CH₃ | −185.0 | −47.6 | Materia prima per composti polimerici; esposizione acuta può avere effetti irritativi. |
| 1-Butene | C₄H₈ | CH₂=CH–CH₂–CH₃ | −185.0 | −6.1 | Idrocarburo insaturo, usato in sintesi organiche; potenziale effetto narcotico lieve. |
| Metilpropene | C₄H₈ | CH₂=C(CH₃)₂ | −140.0 | −6.6 | Conosciuto come isobutene; rilevante nella produzione di polimeri a uso farmaceutico. |
| Etino (acetilene) | C₂H₂ | HC≡CH | −81.8 | −84.0 | Storicamente usato come anestetico; oggi impiegato solo in laboratorio e studi di combustione. |
| Propino | C₃H₄ | HC≡C–CH₃ | −101.5 | −23.2 | Alchino lineare, meno diffuso clinicamente; rilevante come molecola modello. |
| 1-Butino | C₄H₆ | HC≡C–CH₂–CH₃ | −125.9 | 8.1 | Gas insaturo, studiato per la reattività chimica e le implicazioni tossicologiche. |
| 2-Butino | C₄H₆ | CH₃–C≡C–CH₃ | −32.3 | 27.0 | Idrocarburo con triplo legame interno; rilevante in sintesi chimica e ricerca tossicologica. |
| Tabella che descrive le principali proprietà fisiche di alcuni composti appartenenti a queste due classi di idrocarburi. | |||||