Gas reali
Definizione
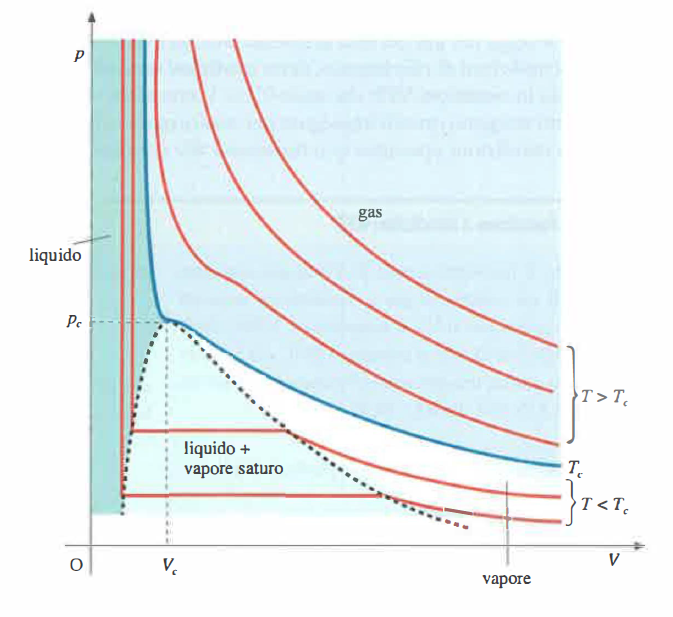
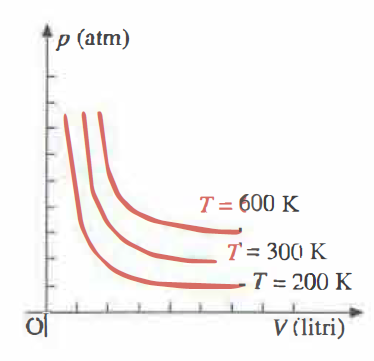
I gas reali mostrano scostamenti sistematici dal modello di gas perfetto discusso in precedenza. Le isoterme sperimentali in un diagramma p-V risultano infatti come in (Figura 05.10-01) e, diversamente dal caso ideale ((Figura 05.10-02), dipendono dalla natura del gas: per specificare numericamente p, V e T è necessario indicare la sostanza considerata. Le curve cambiano in modo qualitativo al variare della temperatura rispetto a un valore caratteristico, la temperatura critica Tc.
Per T < Tc, a grandi volumi (gas rarefatto) l’andamento ricorda quello ideale. Quando si raggiungono le condizioni di condensazione, la pressione rimane costante per un intervallo di volumi: lungo tale tratto coesistono liquido e vapore saturo, e la pressione coincide con la tensione di vapore alla temperatura fissata. Una volta completata la condensazione, l’isoterma diviene molto ripida, riflettendo la ridotta comprimibilità del liquido.
Per T > Tc le isoterme tendono progressivamente a quelle di un gas perfetto man mano che T cresce; oltre Tc la sola compressione non produce liquefazione, quale che sia la pressione applicata. Le temperature critiche di alcuni gas sono riportate in (Tabella 05.10-01). In prossimità di Tc si osservano fenomeni peculiari (ad esempio opalescenza critica) e, per T > Tc, si entra nel dominio dei fluidi supercritici, privi di un confine netto tra “liquido” e “vapore”.
Una descrizione semplice ma efficace del comportamento non ideale è fornita dall’equazione di stato di van der Waals per una mole, ricavata empiricamente:
\[ \left( p + \frac{a}{V^2} \right) (V - b) = R T \]
Dalla formula si ottiene a partire da \(pV = RT\) introducendo due costanti specifiche del gas, a e b, che correggono rispettivamente l’effetto delle interazioni intermolecolari attrattive e del volume proprio delle molecole. Questi parametri si misurano sperimentalmente e riflettono le proprietà microscopiche della sostanza. In forma equivalente: \(p = \frac{RT}{V - b} - \frac{a}{V^2}\):
- Correzione di volume: poiché le molecole occupano spazio, il volume effettivamente disponibile al moto traslazionale è minore del volume del recipiente; il termine \(V - b\) sottrae il cosiddetto covolume b (Figura 05.10-03);
- Correzione di pressione: le forze attrattive tra molecole riducono la pressione misurata sulle pareti rispetto alla sola componente cinetica; per compensare, si somma a p un contributo proporzionale alla densità al quadrato, \(a/V^2\), che cresce al diminuire del volume.
Nel limite di gas diluiti, \(V \gg b\) e \(a/V^2 \to 0\), la (\left( p + \frac{a}{V^2} \right) (V - b) = R T) si riconduce a \(pV = RT\), coerentemente con il comportamento ideale a bassa pressione. Il grado di scostamento dall’idealità si quantifica tramite il fattore di comprimibilità \(Z = \frac{pV}{RT}\), che vale 1 per un gas perfetto e si discosta da 1 per i gas reali in funzione di p e T.
La struttura delle isoterme in (Figura 05.10-01) è coerente con le proprietà critiche. Applicando alla (\left( p + \frac{a}{V^2} \right) (V - b) = R T) le condizioni del punto critico, \[ \left(\frac{\partial p}{\partial V}\right)_T = 0, \quad \left(\frac{\partial^2 p}{\partial V^2}\right)_T = 0, \] si ottiene per una mole: \[ V_c = 3b, \quad p_c = \frac{a}{27 b^2}, \quad T_c = \frac{8a}{27 b R}. \] Da cui, in funzione delle grandezze critiche misurabili: \[ b = \frac{R T_c}{8 p_c}, \qquad a = \frac{27 R^2 T_c^2}{64 p_c}. \] Segue inoltre il valore universale, nel modello di van der Waals, del fattore di comprimibilità critico \(Z_c = \frac{p_c V_c}{R T_c} = \frac{3}{8} = 0{,}375\).
Esempio numerico (valori tipici): per l’anidride carbonica, con \(T_c \approx 304{,}13\ \mathrm{K}\) e \(p_c \approx 7{,}38\ \mathrm{MPa}\), si stimano \[ b \approx \frac{8{,}314 \times 304{,}13}{8 \times 7{,}38 \times 10^6}\ \mathrm{m^3\,mol^{-1}} \approx 4{,}28 \times 10^{-5}\ \mathrm{m^3\,mol^{-1}}, \] \[ a \approx \frac{27 \times (8{,}314)^2 \times (304{,}13)^2}{64 \times 7{,}38 \times 10^6}\ \mathrm{Pa\,m^6\,mol^{-2}} \approx 0{,}365\ \mathrm{Pa\,m^6\,mol^{-2}}. \] A \(T = 320\ \mathrm{K} > T_c\), la CO₂ non può essere liquefatta per sola compressione; a \(T = 300\ \mathrm{K} < T_c\), una compressione isoterma mostra il tratto a pressione quasi costante di coesistenza vapore–liquido, in accordo con la porzione piatta delle isoterme in (Figura 05.10-01).
La dipendenza dalle proprietà molecolari, evidente nella difformità delle isoterme tra sostanze (Figura 05.10-01), spiega perché per T molto alte e pressioni modeste i gas si comportino “quasi ideali”, mentre in prossimità della condensazione emergono deviazioni marcate governate da attrazioni e volume proprio, riassunte nei parametri a e b della \left( p + \frac{a}{V^2} \right) (V - b) = R T.
| Gas | Tc (°C) | Nota |
|---|---|---|
| Azoto (N₂) | –147.1 | Gas inerte, costituente principale dell’aria atmosferica; in medicina usato nei sistemi criogenici. |
| Anidride carbonica (CO₂) | +31.3 | Gas prodotto dal metabolismo; parametro utile per la fisiologia respiratoria e anestesiologia. |
| Ossigeno (O₂) | –118.6 | Fondamentale per la respirazione cellulare; proprietà criogeniche rilevanti in conservazione biologica. |
| Acqua (H₂O) | +374.1 | Riferimento universale, influenza processi fisiologici e termoregolazione. |
| Protossido di azoto (N₂O) | +310.5 | Gas anestetico con utilizzo clinico, noto anche come “gas esilarante”. |
| Aria | –141.0 | Miscela respiratoria naturale, parametro critico in dinamiche atmosferiche e fisiologia polmonare. |
| Elio (He) | –267.9 | Gas inerte usato in risonanza magnetica (RMN) e in miscele respiratorie iperbariche. |
| Idrogeno (H₂) | –240.0 | Gas leggerissimo; studiato per applicazioni sperimentali in medicina iperbarica. |
| Neon (Ne) | –228.7 | Gas nobile con applicazioni criogeniche. |
Temperature critiche dei gas
Valori della temperatura critica per diverse specie gassose.