Radiazione elettromagnetica
Definizione
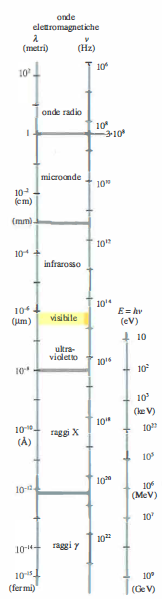
La radiazione elettromagnetica può essere descritta come la propagazione nello spazio di un campo elettrico \( \mathbf{E} \) e di un campo magnetico \( \mathbf{B} \), oscillanti e tra loro ortogonali; la direzione di trasporto dell’energia è perpendicolare a entrambi, il che attesta la natura trasversale delle onde. Nel vuoto la velocità di propagazione è la costante universale \( c \). La classificazione delle radiazioni elettromagnetiche si basa sulla frequenza \( \nu \) (o, in modo equivalente, sulla lunghezza d’onda \( \lambda \) con \( \lambda = c/\nu \)); la corrispondenza tra bande spettrali e frequenza è riportata in (Figura 07.14-01), insieme alla scala energetica dei quanti di radiazione (fotoni) con relazione \( E = h\nu \), dove \( h \) è la costante di Planck. A causa dell’ampiezza dello spettro, in (Figura 07.14-01) l’asse è in scala logaritmica e la regione del visibile occupa solo una piccola porzione dell’intero intervallo.
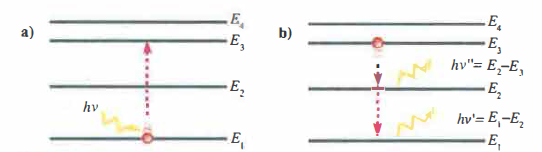
Quando la frequenza è elevata, l’aspetto quantistico (corpuscolare) della radiazione diviene particolarmente evidente, poiché i fotoni possiedono energia più alta. Indipendentemente dalla frequenza, l’emissione e l’assorbimento avvengono sempre per pacchetti di energia discreti, i fotoni. L’assorbimento di un fotone promuove un atomo o una molecola dallo stato fondamentale a uno stato eccitato, trasferendogli integralmente l’energia del quanto (Figura 07.14-02). La successiva diseccitazione (Figura 07.14-02) può avvenire con un’unica transizione oppure mediante una cascata di passaggi verso stati via via più bassi. Alla transizione fra due livelli, indicati con 1 e 2, è associata l’emissione (o l’assorbimento) di un fotone di frequenza determinata da:
\[\nu = \frac{|E_1 - E_2|}{h},\]
dove \(E_1\) ed \(E_2\) sono le energie dei due stati (Figura 07.14-02). Se i livelli energetici sono ben separati, lo spettro emesso o assorbito risulta discreto (spettro a righe); quando invece i livelli sono molto numerosi e ravvicinati, lo spettro appare praticamente continuo. Nel caso atomico, le frequenze di riga sono caratteristiche e consentono l’identificazione della specie; per le molecole la struttura è più articolata, in ragione della presenza di sottostrutture vibrazionali e rotazionali accoppiate alle transizioni elettroniche. Le transizioni atomiche e molecolari interessano tipicamente l’intervallo dall’infrarosso fino ai raggi X, mentre le radiazioni \( \gamma \) sono associate a transizioni interne ai nuclei atomici.
Dal punto di vista energetico e della propagazione, il flusso di energia istantaneo è descritto dal vettore di Poynting \( \mathbf{S} \propto \mathbf{E} \times \mathbf{B} \), diretto lungo la direzione d’avanzamento dell’onda. La linea spettrale osservata può risultare allargata per diversi meccanismi, che preservano la quantizzazione ma modificano il profilo osservabile:
- allargamento naturale, legato al principio di indeterminazione tra energia e tempo;
- allargamento Doppler, dovuto al moto termico delle particelle assorbenti o emittenti;
- allargamento per collisioni (o pressione), associato a interazioni tra particelle.
Sia i raggi X sia i raggi \( \gamma \) possono essere generati artificialmente; all’estremo opposto dello spettro, onde radio e microonde si ottengono comunemente tramite circuiti e risonatori oscillanti.