Materia e proprietà
Definizione
Le proprietà descrivono il comportamento e le caratteristiche della materia. In ambito chimico si distinguono proprietà fisiche e proprietà chimiche, utili per identificare, confrontare e classificare sostanze e materiali. In parallelo, la materia può essere organizzata secondo la sua composizione in sostanze pure ed in miscele, il che consente di prevederne molte caratteristiche e modalità di separazione sulla base di principi fisici e chimici.
Un’indagine sperimentale genera dati, cioè misure o osservazioni elementari (ad esempio: massa, lunghezza, volume, tempo, temperatura, energia). Un singolo dato è l’esito di una misura isolata; il risultato, invece, deriva spesso dall’elaborazione coerente di più dati, talvolta corretti per fattori di influenza e inquadrati da incertezze e condizioni operative.
Distinguere tra dato e risultato è cruciale: la perdita di massa di un campione per riscaldamento, per esempio, è un risultato che si ottiene combinando misure di massa a tempi diversi, conoscendo temperatura, pressione, umidità relativa e caratteristiche del contenitore. Senza registrare tali variabili, l’interpretazione resta ambigua e la riproducibilità diminuisce.
Si consideri un’analisi della disidratazione di un sale idrato lasciato all’aria: pesare il campione a intervalli regolari, annotare la temperatura ambiente, l’umidità e il tempo di esposizione consente di calcolare una velocità di perdita di massa (per esempio, espressa in g·min⁻¹) a partire da coppie di dati massa–tempo. In questo caso, i dati sono le singole pesate e i tempi corrispondenti; il risultato è la funzione che descrive la variazione di massa nel tempo, comprensiva di incertezze e condizioni sperimentali.
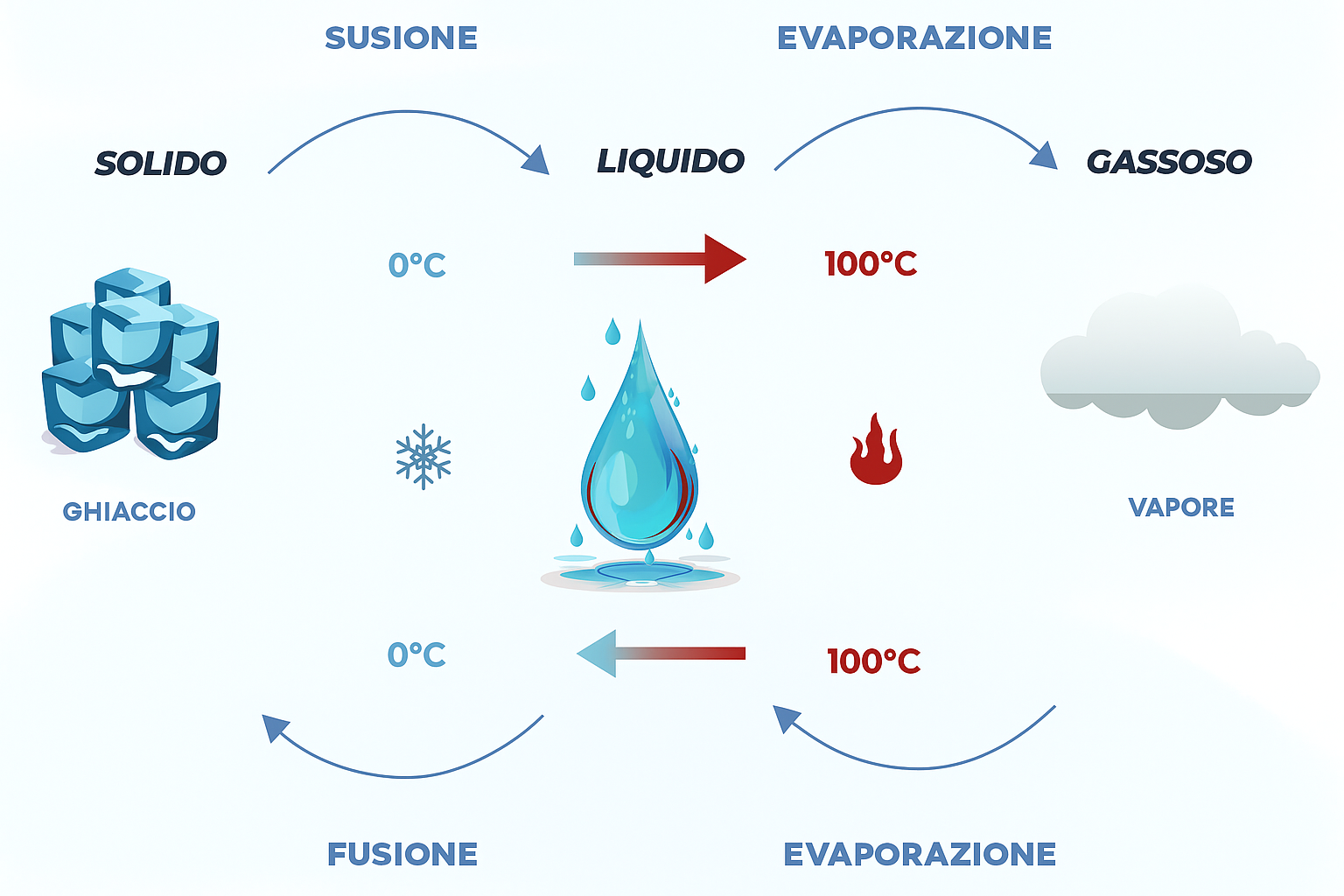
La materia si presenta prevalentemente in tre stati: gassoso, liquido e solido. Le differenze fra questi stati emergono sia a livello macroscopico (forma e volume) sia su scala microscopica (distanze tra particelle e intensità delle interazioni). In generale, le forze attrattive tra particelle sono massime nei solidi, intermedie nei liquidi e minime nei gas:
- Gas: non possiedono forma né volume propri, sono altamente comprimibili e si espandono fino a occupare interamente il contenitore; le particelle sono molto distanti e in moto disordinato;
- Liquidi: hanno volume definito ma non forma propria, assumendo quella del recipiente; sono poco comprimibili e le particelle sono vicine, con libertà di scorrere le une sulle altre;
- Solidi: dispongono di forma e volume propri; sono sostanzialmente incomprimibili e le particelle sono strettamente impaccate, con disposizione spesso regolare (solidi cristallini) o, talora, priva di ordine a lungo raggio (solidi amorfi).
L’acqua offre un esempio paradigmatico di sostanza che, in un ristretto intervallo di temperatura, può trovarsi nei tre stati di aggregazione (Figura 01.02-01). Il passaggio da ghiaccio ad acqua liquida o da acqua a vapore costituisce una trasformazione fisica: cambia l’aspetto e lo stato, ma non la composizione chimica, che resta H₂O. Il congelamento successivo riporta il sistema allo stato solido originario, mostrando la reversibilità del processo.
Le proprietà fisiche sono misurabili senza modificare l’identità della sostanza: punti di fusione ed ebollizione, densità, indice di rifrazione, conducibilità termica ed elettrica, capacità termica, solubilità. La misura del punto di fusione del ghiaccio o del punto di ebollizione dell’acqua è una caratterizzazione fisica, utile per identificare e confrontare campioni. Differenze in proprietà fisiche costituiscono la base per separazioni come distillazione, filtrazione, cristallizzazione o cromatografia (Figura 01.02-02), nelle quali non intervengono reazioni chimiche ma solo cambiamenti di stato o di distribuzione tra fasi.
Le proprietà chimiche descrivono la tendenza di una sostanza a trasformarsi in un’altra mediante reazioni che cambiano la disposizione degli atomi e la natura dei legami. Esempi tipici sono la combustione, l’ossidazione, l’idrolisi, l’acidità o basicità, la capacità di complessazione.
La fotosintesi è un processo chimico in cui anidride carbonica e acqua reagiscono, in presenza di luce, per generare glucosio e ossigeno, secondo la stechiometria:
\[ 6\,CO_2 + 6\,H_2O \xrightarrow{\text{luce}} C_6H_{12}O_6 + 6\,O_2 \]
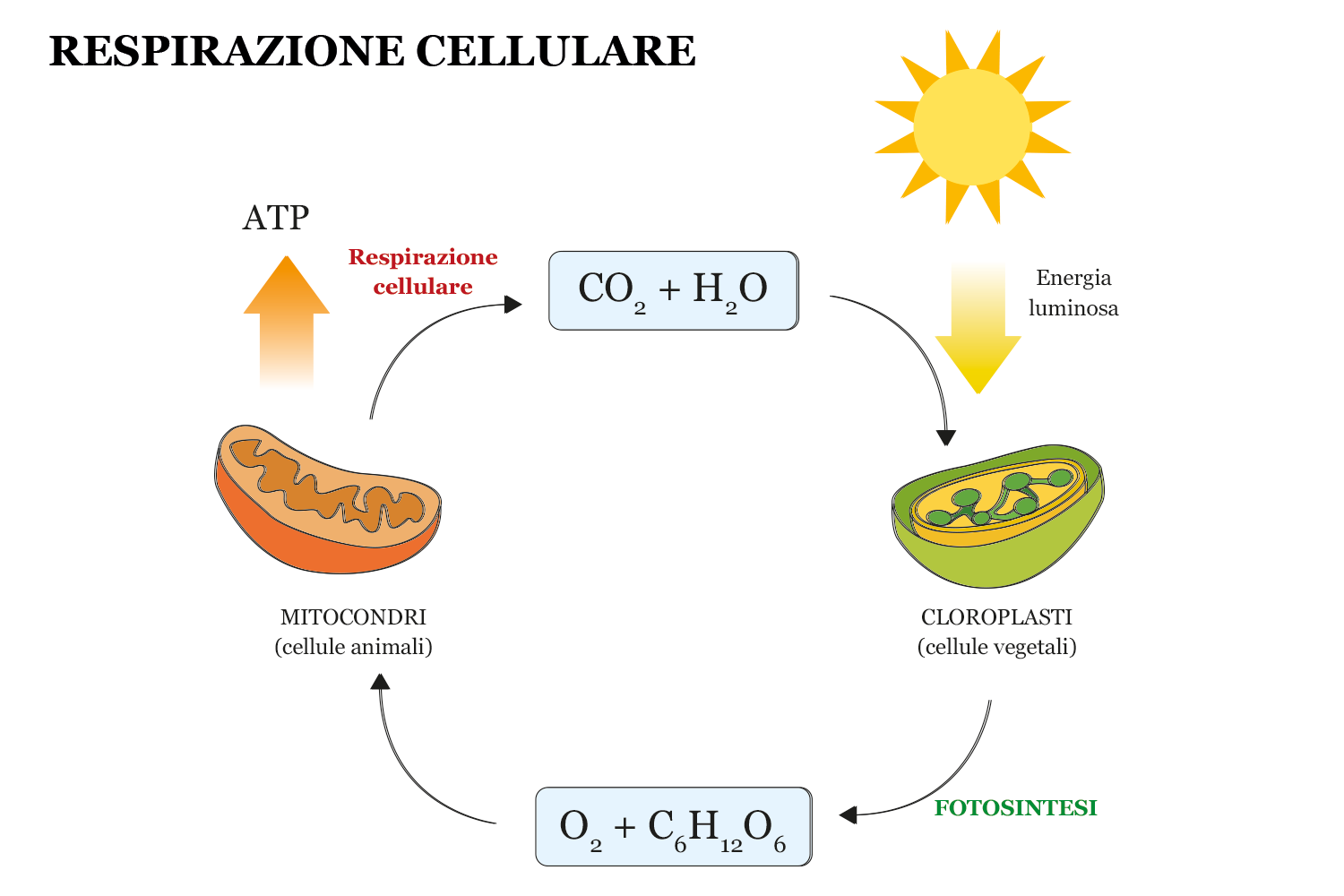 |
| Ciclo fotosintesi–respirazione cellulare |
Qui reagenti e prodotti presentano proprietà macroscopiche differenti: CO₂ e O₂ sono gas a temperatura ambiente, l’acqua è liquida, il glucosio è un solido cristallino. La possibilità della CO₂ di partecipare a questa trasformazione, in condizioni opportune, rappresenta una sua proprietà chimica. Si tratta di una trasformazione chimica perché la composizione cambia e compaiono nuove sostanze con identità diversa.
Le proprietà della materia si distinguono anche per la loro dipendenza dalla quantità di campione. Le proprietà intensive non variano con l’estensione del sistema; quelle estensive sono proporzionali alla quantità di sostanza considerata:
- Proprietà intensive: densità, punto di fusione, punto di ebollizione, pressione di vapore, indice di rifrazione, densità relativa (o gravità specifica);
- Proprietà estensive: massa, volume, quantità di moto, energia totale, carica netta.
La densità è definita da \( \rho = \frac{m}{V} \) ed è intensiva: due campioni di rame da 5,0 g e 50 g hanno la stessa densità, pari a 8,96 g·cm⁻³, pur avendo masse e volumi differenti. La densità relativa è il rapporto tra la densità di una sostanza e quella di un riferimento (spesso l’acqua a 4 °C), ed è priva di unità. Al contrario, massa e volume dipendono dalla quantità: 1,0 g d’argento e 1,0 kg d’argento differiscono sia per valore sia per impiego pratico.
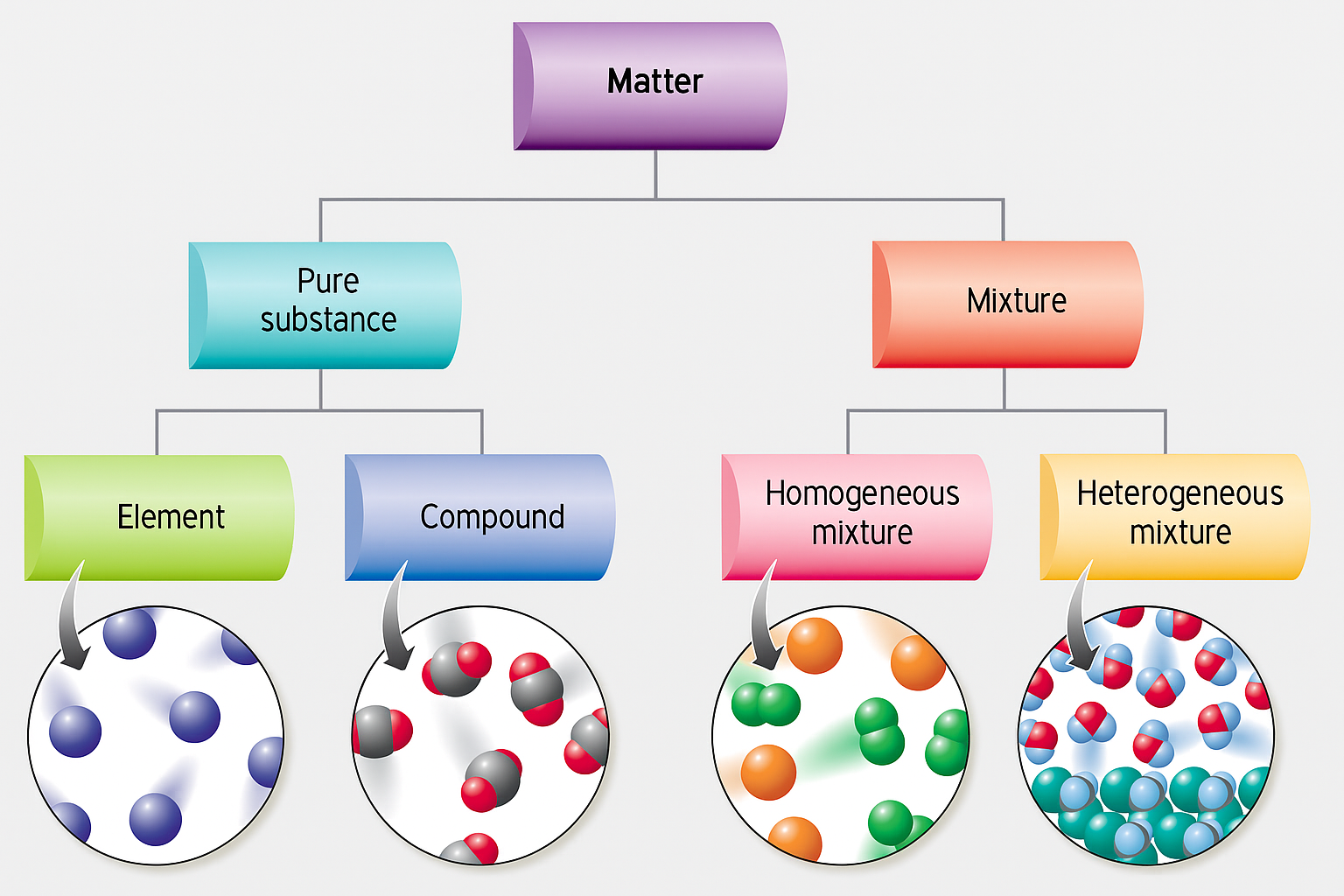
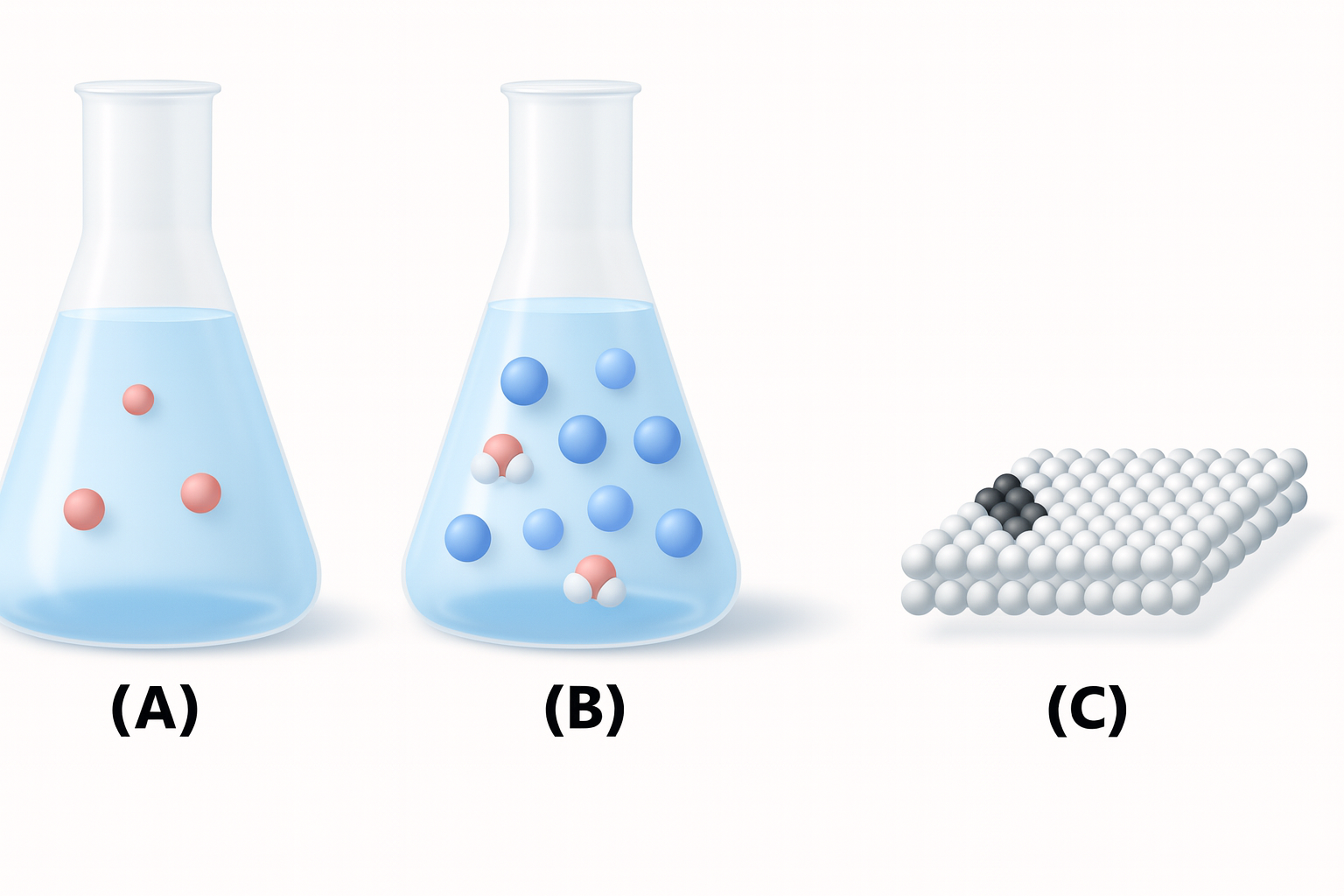
La classificazione basata sulla composizione (Figura 01.02-03) distingue tra sostanze pure e miscele. Una sostanza pura possiede composizione costante e proprietà definite; rientrano in questa categoria gli elementi e i composti. Un elemento non è decomponibile per via chimica in sostanze più semplici (esempi: H₂, O₂, Fe). Un composto nasce dalla combinazione in proporzioni fisse di due o più elementi con formazione di specie chimiche nuove (esempi: H₂O, NaCl, CO₂).
Una miscela è un insieme di due o più sostanze pure che coesistono mantenendo la propria identità chimica; la composizione è variabile. Le miscele possono essere:
- Omogenee (soluzioni), con composizione uniforme e un’unica fase macroscopica; esempi: aria, soluzioni acquose di etanolo, leghe come l’ottone;
- Eterogenee, con composizione non uniforme e più fasi distinguibili; esempi: acqua e olio, sospensioni solide in liquidi, materiali compositi come il cemento.
Le differenze di proprietà fisiche tra i componenti (solubilità, volatilità, dimensione delle particelle, magnetismo) consentono la separazione con metodi fisici non distruttivi, quali distillazione, filtrazione, decantazione, estrazione o magnetoseparazione (Figura 01.02-04). In questo modo, la composizione del sistema cambiata è solo quella macroscopica (distribuzione dei componenti), non l’identità molecolare delle sostanze separate.