Legge periodica e tavola periodica
Definizione
Nel 1869 Dmitrij Mendeleev in Russia e Lothar Meyer in Germania, indipendentemente, allinearono gli elementi in ordine di massa atomica crescente, evidenziando che elementi con comportamenti affini ricorrono a intervalli regolari e possono essere raggruppati in una tavola. La legge periodica, nella formulazione originaria di Mendeleev, afferma che le proprietà degli elementi variano in modo ricorrente quando gli elementi sono ordinati per peso atomico. La tavola periodica (Figura 01.09-01) visualizza questa regolarità. Con l’affermarsi del modello atomico e della struttura a livelli dell’elettrone, è emerso che le proprietà chimico-fisiche dipendono dalla configurazione elettronica e, quindi, dalla posizione nella tavola. Imparare a leggere tale “mappa” consente di anticipare configurazioni elettroniche, stati di ossidazione, dimensioni atomiche e tendenze reattive.
La nozione di periodicità si coglie bene lungo una riga: nella seconda riga, dal litio (Li) al neon (Ne), il passaggio da sinistra a destra corrisponde a cambiamenti sistematici di carattere chimico e fisico; scendendo nella colonna del litio si incontrano elementi (come il sodio, Na) con proprietà analoghe. Questa ricorrenza attraversa l’intera tavola. La svolta concettuale del XX secolo, dovuta alle misure spettroscopiche di H. G. J. Moseley, ha mostrato che la sequenza naturale degli elementi è data dal numero atomico \(Z\) (numero di protoni), non dalla massa. La legge periodica moderna si esprime dunque così: le proprietà degli elementi sono funzioni periodiche di \(Z\). Ordinando gli elementi per numero di protoni crescente, i pattern di proprietà si ripresentano a intervalli regolari, risolvendo anche le apparenti anomalie dell’ordinamento per massa (come la coppia Te/I). Notevole fu la capacità predittiva della tavola mendeleeviana: vennero previsti spazi e proprietà di elementi non ancora isolati, poi effettivamente scoperti.
In ambito biochimico non tutti gli elementi rivestono la stessa rilevanza. La (Tabella 01.09-01) riporta i venti elementi più significativi per i sistemi viventi, con simboli e brevi funzioni: leggere la tavola come una carta stradale, più che come un elenco da memorizzare, consente di trasferire quanto appreso su un elemento all’intera famiglia cui appartiene.
| Elemento | Simbolo | Ruolo biologico / Importanza clinica |
|---|---|---|
| Idrogeno | H | Costituente essenziale delle molecole organiche e dell’acqua |
| Carbonio | C | Struttura portante delle biomolecole (carboidrati, lipidi, proteine, acidi nucleici) |
| Ossigeno | O | Fondamentale per i processi ossidativi e la respirazione cellulare |
| Azoto | N | Presente in amminoacidi, basi azotate e proteine |
| Fosforo | P | Componente dei fosfolipidi, degli acidi nucleici e dei sistemi energetici (ATP) |
| Zolfo | S | Costituente di alcuni amminoacidi e cofattori enzimatici |
| Potassio | K | Elettrolita chiave nella regolazione del bilancio idrico e della trasmissione nervosa |
| Sodio | Na | Regola l’equilibrio osmotico e la conduzione nervosa |
| Cloro | Cl | Presente nei fluidi corporei, partecipa al mantenimento del pH e dell’equilibrio idro-elettrolitico |
| Calcio | Ca | Essenziale per la struttura ossea, la coagulazione e la contrazione muscolare |
| Magnesio | Mg | Cofattore enzimatico e regolatore della funzione neuromuscolare |
| Zinco | Zn | Coinvolto in numerosi enzimi e nella risposta immunitaria |
| Stronzio | Sr | Associato al metabolismo osseo |
| Ferro | Fe | Componente dell’emoglobina e di enzimi respiratori |
| Rame | Cu | Cofattore di enzimi ossidativi, partecipa alla formazione del collagene |
| Cobalto | Co | Presente nella vitamina B12, essenziale per la sintesi degli eritrociti |
| Manganese | Mn | Attivatore enzimatico nel metabolismo dei carboidrati e delle proteine |
| Molibdeno | Mo | Cofattore di enzimi coinvolti nel metabolismo dei solfati e delle purine |
| Selenio | Se | Antiossidante, presente nella glutatione perossidasi |
| Litio | Li | Tracce fisiologiche, usato in ambito clinico per disturbi psichiatrici |
| Cadmio | Cd | Metallo pesante, tossico per organi e tessuti |
| Mercurio | Hg | Metallo pesante con effetti neurotossici |
| Piombo | Pb | Metallo pesante con azione tossica sul sistema nervoso e midollo osseo |
Elementi fondamentali nei sistemi biologici
Sintesi dei principali elementi coinvolti nei processi biologici.
L’ordinamento per colonne (gruppi) ha conosciuto diverse convenzioni. Fino agli anni ’80 in Nord America e in Russia si usavano numeri romani con A per i “rappresentativi” e B per i “di transizione”, mentre in altre aree le lettere A e B venivano assegnate in modo difforme, creando disallineamenti tra tavole. Nel 1983 la IUPAC (International Union of Pure and Applied Chemistry) raccomandò di numerare i gruppi progressivamente da 1 a 18, superando i sistemi precedenti. Nella pratica, è ancora possibile incontrare tutti e tre i sistemi, fatto che può disorientare. La numerazione è però solo una legenda: l’informazione decisiva resta la struttura stessa della tavola e le corrispondenze elettroniche che essa sintetizza.
Un periodo è una riga orizzontale; la tavola moderna comprende sette periodi che contengono rispettivamente 2, 8, 8, 18, 18, 32 e 32 elementi. Le serie dei lantanidi e degli attinidi appartengono al sesto e al settimo periodo, rispettivamente, ma per praticità tipografica sono riportate a parte: i lantanidi si inseriscono tra lantanio (La, \(Z=57\)) e afnio (Hf, \(Z=72\)), gli attinidi tra attinio (Ac, \(Z=89\)) e rutherfordio (Rf, \(Z=104\)). Le colonne verticali sono i gruppi o famiglie: gli elementi della stessa colonna condividono pattern elettronici di valenza e, di conseguenza, molte proprietà chimiche e fisiche. Nella terminologia tradizionale, i gruppi 1, 2 e 13–18 sono “rappresentativi” (A), mentre i gruppi 3–12 costituiscono i metalli di transizione (B); lantanidi e attinidi sono talvolta detti elementi di transizione interna.
Alcuni gruppi hanno nomi storici: il gruppo 1 (IA) raccoglie i metalli alcalini, il gruppo 2 (IIA) i metalli alcalino-terrosi, il gruppo 17 (VIIA) gli alogeni, il gruppo 18 (VIIIA) i gas nobili. La tavola può essere letta anche per “blocchi” orbitalici, che spiegano le lunghezze dei periodi:
- blocco s: due colonne, caratterizzate da configurazioni di valenza \(n s^1\) (gruppo 1) e \(n s^2\) (gruppo 2);
- blocco p: sei colonne (gruppi 13–18) con riempimento progressivo \(n p^{1-6}\);
- blocco d: dieci colonne (gruppi 3–12) con configurazioni \((n-1)d^{1-10}\, n s^{0-2}\);
- blocco f: quattordici elementi per ciascuna delle due serie, con riempimento \((n-2)f^{1-14}\).
Questa organizzazione rende conto delle periodicità di stati di ossidazione, raggi atomici e reattività. Ad esempio, lungo un gruppo si mantiene il conteggio degli elettroni di valenza (p.es. alogeni: \(n s^2 n p^5\)), mentre lungo un periodo tali elettroni aumentano fino al completamento dell’ottetto.
I metalli si distinguono per la tendenza a cedere elettroni formando cationi, per lucentezza, malleabilità e buona conducibilità termica ed elettrica; quasi tutti sono solidi a temperatura ambiente, salvo il mercurio. I non metalli, in generale, tendono ad acquistare elettroni o a condividere coppie elettroniche, presentano scarsa conducibilità e si trovano come gas, liquidi o solidi fragili. Tra i due domini si colloca una fascia a “scalino” dalla zona del boro (B) verso il polonio (Po) e l’astato (At): su questo confine si collocano i metalloidi, che esibiscono proprietà intermedie e spesso comportamento semiconduttivo. Sono comunemente considerati metalloidi: boro (B), silicio (Si), germanio (Ge), arsenico (As), antimonio (Sb) e tellurio (Te). Gli elementi superpesanti sintetici, come tennessine (Ts) e oganesson (Og), hanno interesse limitato per la chimica di base.
La distribuzione metallo/non metallo segue tendenze regolari: il carattere metallico diminuisce procedendo da sinistra a destra in un periodo e aumenta scendendo lungo un gruppo. Una razionalizzazione utile si basa sulla carica nucleare efficace \(Z_\mathrm{eff}\): lungo il periodo \(Z_\mathrm{eff}\) cresce, il raggio atomico si riduce e risulta più difficile perdere elettroni (diminuisce il carattere metallico), mentre aumenta l’attitudine a catturarli; scendendo nel gruppo, l’aumento del raggio e la schermatura degli strati interni favoriscono la cessione di elettroni.
Il numero atomico \(Z\) è il conteggio dei protoni nel nucleo, pari alla carica positiva nucleare in unità elementari; in un atomo neutro vale anche il numero di elettroni. È \(Z\) a determinare l’identità dell’elemento e l’ordinamento nella tavola. La moderna legge periodica si può sintetizzare come \(P(Z+N)=P(Z)\), dove \(P\) rappresenta una proprietà che si ripete con periodicità al crescere di \(Z\), una volta completati i riempimenti di strato.
Accanto a \(Z\), le tavole riportano la massa atomica relativa \(A_r\), cioè la media ponderata delle masse isotopiche rispetto allo standard carbonio-12. Se un elemento \(E\) possiede isotopi di massa \(m_i\) con abbondanze frazionarie \(x_i\), allora \[ A_r(E) = \sum_i x_i\, m_i. \] Di conseguenza \(A_r\) non è in generale un intero: per esempio, il cloro presenta \(A_r \approx 35,45\) poiché è una miscela naturale di isotopi con masse vicine a 35 e 37. Si distingue \(A_r\) dal numero di massa \(A = Z + N\), definito per il singolo isotopo come somma di protoni e neutroni.
La tavola periodica riporta comunemente \(Z\) e \(A_r\), ma versioni più dettagliate includono configurazioni elettroniche, raggi atomici e ionici, elettronegatività, potenziali di ionizzazione, nonché stati di ossidazione più frequenti, molto utili per prevedere formule e reazioni.
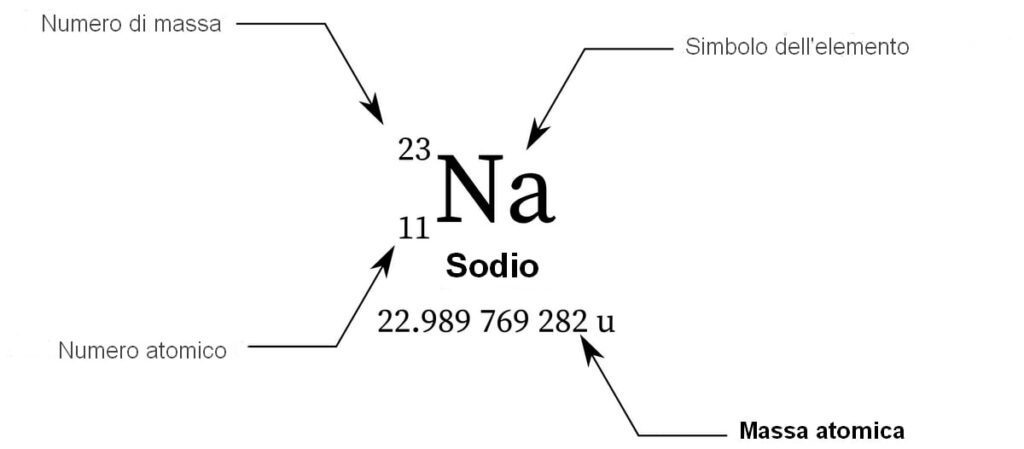 |
| Sodio – simbolo, numero atomico e massa atomica |
Come guida pratica, la tavola periodica (Figura 01.09-01) può essere letta come una carta di correlazioni tra struttura elettronica e proprietà: le informazioni ricavate per un elemento si estendono, con le dovute cautele, all’intero gruppo cui appartiene, principio che rende la tavola uno strumento sintetico e predittivo per tutta la chimica di base, dalla stechiometria al legame chimico, fino alla reattività inorganica e bioinorganica delineata nella (Tabella 01.09-01).
| Elemento | Simbolo | Ruolo biologico / Importanza clinica |
|---|---|---|
| Idrogeno | H | Costituente essenziale delle molecole organiche e dell’acqua |
| Carbonio | C | Struttura portante delle biomolecole (carboidrati, lipidi, proteine, acidi nucleici) |
| Ossigeno | O | Fondamentale per i processi ossidativi e la respirazione cellulare |
| Azoto | N | Presente in amminoacidi, basi azotate e proteine |
| Fosforo | P | Componente dei fosfolipidi, degli acidi nucleici e dei sistemi energetici (ATP) |
| Zolfo | S | Costituente di alcuni amminoacidi e cofattori enzimatici |
| Potassio | K | Elettrolita chiave nella regolazione del bilancio idrico e della trasmissione nervosa |
| Sodio | Na | Regola l’equilibrio osmotico e la conduzione nervosa |
| Cloro | Cl | Presente nei fluidi corporei, partecipa al mantenimento del pH e dell’equilibrio idro-elettrolitico |
| Calcio | Ca | Essenziale per la struttura ossea, la coagulazione e la contrazione muscolare |
| Magnesio | Mg | Cofattore enzimatico e regolatore della funzione neuromuscolare |
| Zinco | Zn | Coinvolto in numerosi enzimi e nella risposta immunitaria |
| Stronzio | Sr | Associato al metabolismo osseo |
| Ferro | Fe | Componente dell’emoglobina e di enzimi respiratori |
| Rame | Cu | Cofattore di enzimi ossidativi, partecipa alla formazione del collagene |
| Cobalto | Co | Presente nella vitamina B12, essenziale per la sintesi degli eritrociti |
| Manganese | Mn | Attivatore enzimatico nel metabolismo dei carboidrati e delle proteine |
| Molibdeno | Mo | Cofattore di enzimi coinvolti nel metabolismo dei solfati e delle purine |
| Selenio | Se | Antiossidante, presente nella glutatione perossidasi |
| Litio | Li | Tracce fisiologiche, usato in ambito clinico per disturbi psichiatrici |
| Cadmio | Cd | Metallo pesante, tossico per organi e tessuti |
| Mercurio | Hg | Metallo pesante con effetti neurotossici |
| Piombo | Pb | Metallo pesante con azione tossica sul sistema nervoso e midollo osseo |
Elementi fondamentali nei sistemi biologici
Sintesi dei principali elementi coinvolti nei processi biologici.









