Proprietà basate sulla struttura elettronica e sulla geometria molecolare
Definizione
Le interazioni intramolecolari corrispondono ai legami chimici che tengono uniti gli atomi in una molecola e ne determinano disposizione spaziale, distribuzione elettronica e polarità. Le interazioni intermolecolari, invece, agiscono tra molecole distinte e, pur scaturendo dalla geometria e dalla ripartizione delle cariche all’interno delle singole specie, governano fenomeni macroscopici come solubilità, tensione di vapore, nonché temperature di ebollizione e di fusione. La distinzione è cruciale: variazioni nella struttura elettronica e nella forma molecolare modificano le forze tra particelle, e da esse derivano differenze misurabili nelle proprietà fisiche. Nei paragrafi seguenti vengono discusse le principali conseguenze di tali forze su solubilità e transizioni di fase (ebollizione e fusione).
La solubilità è la massima quantità di soluto che può sciogliersi in una data quantità di solvente a una temperatura specificata, fino al raggiungimento dell’equilibrio. In termini termodinamici, la miscela è favorita quando la variazione di energia libera è negativa: \( \Delta G_{\mathrm{sol}} = \Delta H_{\mathrm{sol}} - T \Delta S_{\mathrm{sol}} < 0 \). La regola empirica “il simile scioglie il simile” sintetizza l’osservazione che sostanze con polarità comparabile risultano generalmente miscibili, poiché possono instaurare interazioni di intensità analoga (dipolo–dipolo, legami a idrogeno, forze di dispersione) riducendo l’energia del sistema senza penalità entalpiche elevate.
La compatibilità tra soluto e solvente è spesso spiegata considerando la natura delle principali forze intermolecolari coinvolte:
- forze di dispersione (London), presenti universalmente e crescenti con la polarizzabilità e la massa molare;
- interazioni dipolo–dipolo, rilevanti tra molecole permanentemente polari;
- legami a idrogeno, particolarmente forti quando un H è legato a F, O o N ed è accettato da un doppietto elettronico su un eteroatomo;
- interazioni ione–dipolo, determinanti quando ioni si solvatano in solventi polari;
- effetto idrofobico e tensione interfacciale, che disfavoriscono l’esposizione di superfici apolari in solventi fortemente coordinanti come l’acqua.
Esempio I: ammoniaca in acqua
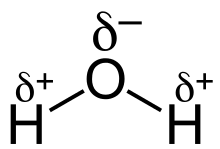
L’ammoniaca è altamente solubile in acqua, poiché entrambe le molecole sono polari e possono formare legami a idrogeno reciproci. Nella molecola d’acqua, l’ossigeno porta una parziale carica negativa (\(\delta^-\)) e gli idrogeni parziali cariche positive (\(\delta^+\)), mentre in NH3 l’azoto è relativamente \(\delta^-\) e gli idrogeni \(\delta^+\). Le attrazioni tra il sito \(\delta^-\) dell’azoto e gli H \(\delta^+\) dell’acqua, e tra l’ossigeno \(\delta^-\) dell’acqua e gli H \(\delta^+\) dell’ammoniaca, generano una rete di interazioni che favorisce la dispersione delle molecole di NH3 nel solvente, fino a ottenere una soluzione omogenea (Figura 01.17-01). Oltre alle interazioni fisiche, in acqua si instaura anche un equilibrio acido–base che porta alla formazione di ioni ammonio e idrossido, contribuendo ulteriormente alla solubilizzazione a diluizione moderata.
 |
| Formazione dello ione ammonio (NH₄⁺) per protonazione dell’ammoniaca |
 |
| Geometria molecolare dell’ammoniaca (NH₃) con angolo di legame e lunghezza di legame |
La miscibilità è favorita sia dall’elevata costante dielettrica dell’acqua, che stabilizza specie cariche e dipolari, sia dalla possibilità di stabilire molteplici legami a idrogeno incrociati.
Esempio II: olio e acqua
L’olio, formato prevalentemente da catene idrocarburiche apolari, manifesta interazioni di dispersione tra le proprie molecole, ma non presenta siti polari in grado di interagire efficacemente con l’acqua. Quest’ultima, fortemente polare e capace di un’estesa rete di legami a idrogeno, “preferisce” interagire con se stessa, mentre l’inclusione di specie apolari comporta un costo entalpico e la formazione di interfacce ad alta tensione superficiale. Ne risulta una scarsa solubilità reciproca: l’olio resta separato e, essendo meno denso, forma uno strato galleggiante (Figura 01.17-02). Processi di emulsificazione richiedono tensioattivi che riducano la tensione interfacciale e stabilizzino goccioline disperse.
L’ebollizione si verifica quando la pressione di vapore del liquido eguaglia la pressione esterna; l’energia fornita serve a superare le attrazioni intermolecolari e a promuovere il passaggio alla fase gassosa. A parità di condizioni, forze intermolecolari più intense implicano un’entalpia di vaporizzazione maggiore e quindi una temperatura di ebollizione più elevata. La massa molare e la forma delle molecole concorrono significativamente: molecole più pesanti o più facilmente polarizzabili presentano forze di dispersione più forti e, di norma, punti di ebollizione più alti; a parità di massa, strutture allungate con maggiore superficie di contatto bollono a temperature superiori rispetto a isomeri ramificati.
Un’analogia vale per la fusione: la transizione da solido a liquido richiede di indebolire le interazioni che stabilizzano il reticolo. Nei solidi molecolari, legami a idrogeno e interazioni dipolari più forti innalzano i punti di fusione. Per i solidi ionici, la situazione è più articolata: le temperature di fusione riflettono l’energia reticolare, che dipende dalla carica degli ioni, dalle loro dimensioni e dalla struttura cristallina. In sistemi covalenti estesi (reticoli come diamante o quarzo), i punti di fusione sono molto elevati per via dei legami covalenti direzionali estesi in tre dimensioni.
Fattori principali che influenzano i punti di ebollizione e di fusione:
- intensità delle forze intermolecolari: legami a idrogeno e interazioni dipolo–dipolo innalzano le temperature di transizione;
- massa molare e polarizzabilità: valori maggiori aumentano le forze di dispersione;
- geometria e area superficiale: molecole più estese o meno ramificate interagiscono più efficacemente;
- capacità di impaccamento cristallino: solidi con impaccamento efficiente fondono più in alto;
- natura del legame nel solido: ionico, covalente reticolare, metallico o molecolare determinano scale di temperatura molto diverse.
In sintesi, composti polari o capaci di legami a idrogeno mostrano, a parità di massa molare, temperature di ebollizione e fusione superiori rispetto a sostanze apolari analoghe. Valori rappresentativi per differenti classi di sostanze sono riportati nella (Tabella 01.17-01).
| Formula (nome) | Tipo di legame | Punto di fusione (°C) | Punto di ebollizione (°C) | Nota biochimica |
|---|---|---|---|---|
| N₂ (azoto) | Covalente non polare | –210 | –196 | Gas inerte, fondamentale per l’atmosfera terrestre |
| O₂ (ossigeno) | Covalente non polare | –219 | –183 | Indispensabile per la respirazione cellulare |
| NH₃ (ammoniaca) | Covalente polare | –78 | –33 | Molecola polare, coinvolta nel metabolismo azotato |
| H₂O (acqua) | Covalente polare | 0 | 100 | Solvente biologico universale, base della vita |
| NaCl (cloruro di sodio) | Ionico | 801 | 1413 | Essenziale per l’equilibrio idro-elettrolitico |
| KBr (bromuro di potassio) | Ionico | 730 | 1435 | Impiegato in diagnostica e come fonte di potassio |
| CO₂ (anidride carbonica) | Covalente non polare | –56 | –78 (sublima) | Molecola chiave nel metabolismo cellulare e nell’equilibrio acido-base |
| H₂S (idrogeno solforato) | Covalente polare | –85 | –60 | Gas tossico, presente in piccoli quantitativi nei tessuti |
Punti di fusione ed ebollizione e tipologia di legame
Valori di fusione ed ebollizione di diversi composti messi in relazione con la natura del legame chimico.






:max_bytes(150000):strip_icc()/GettyImages-1073482368-d3a7e8a37a3449cb842c3d134320ba38.jpg)



