I legami covalenti polari nelle molecole di acqua determinano la formazione di legami idrogeno
Definizione
La caratteristica che più distingue i viventi dalla materia inerte è la capacità di generare e mantenere ordine locale pur in un contesto fisico in cui predomina la tendenza all’aumento del disordine. In termini termodinamici, i sistemi biologici si comportano come strutture aperte e dissipative: importano nutrienti ed energia, trasformano la materia, ed esportano calore e prodotti di scarto, così che l’entropia complessiva dell’ambiente aumenti mentre la loro organizzazione interna si conserva. In simboli, ciò avviene in accordo con la seconda legge, per cui \( \Delta S_{\text{universo}} \ge 0 \).
Per sostenere tale ordine, le cellule mantengono un flusso incessante di reazioni chimiche che previene il decadimento spontaneo dei componenti e soddisfa le esigenze metaboliche. Parte di queste trasformazioni converte o demolisce piccole molecole organiche — amminoacidi, monosaccaridi, nucleotidi, acidi grassi — per generare energia utilizzabile e intermedi metabolici; altre reazioni impiegano tali unità come blocchi costruttivi per sintetizzare macromolecole e strutture complesse, tra cui proteine, acidi nucleici, polisaccaridi e lipidi di membrana, dalle quali derivano le proprietà funzionali dei sistemi viventi. Ogni cellula opera come un micro-reattore chimico in cui avvengono milioni di trasformazioni al secondo, alimentate da una doppia fornitura: una sorgente di atomi (i nutrienti) e una sorgente di energia chimica, entrambe in ultima analisi riconducibili alla materia non vivente e ai flussi energetici dell’ambiente.
Molte delle reazioni necessarie alla vita, in assenza di catalisi, procederebbero a velocità trascurabili alle temperature fisiologiche. L’efficiente svolgimento delle vie metaboliche è reso possibile da proteine specializzate, gli enzimi, che abbassano l’energia di attivazione \(E_a\) e incrementano enormemente la velocità di reazione senza alterarne l’equilibrio termodinamico né il valore di \(\Delta G\). Ogni enzima è altamente specifico per i propri substrati e per il tipo di trasformazione chimica che catalizza. Le reazioni enzimatiche sono spesso organizzate in sequenze in cui il prodotto di una tappa diviene il substrato della successiva (Figura 01.11-01); sequenze differenti si intersecano e comunicano tra loro, generando reti complesse. L’esigenza di catalisi non è un limite ma un vantaggio funzionale, poiché permette un controllo fine del metabolismo — l’insieme coordinato di tutte le reazioni che consentono sopravvivenza, accrescimento e riproduzione — tramite regolazioni allosteriche, compartimentalizzazione subcellulare e modulazioni covalenti.
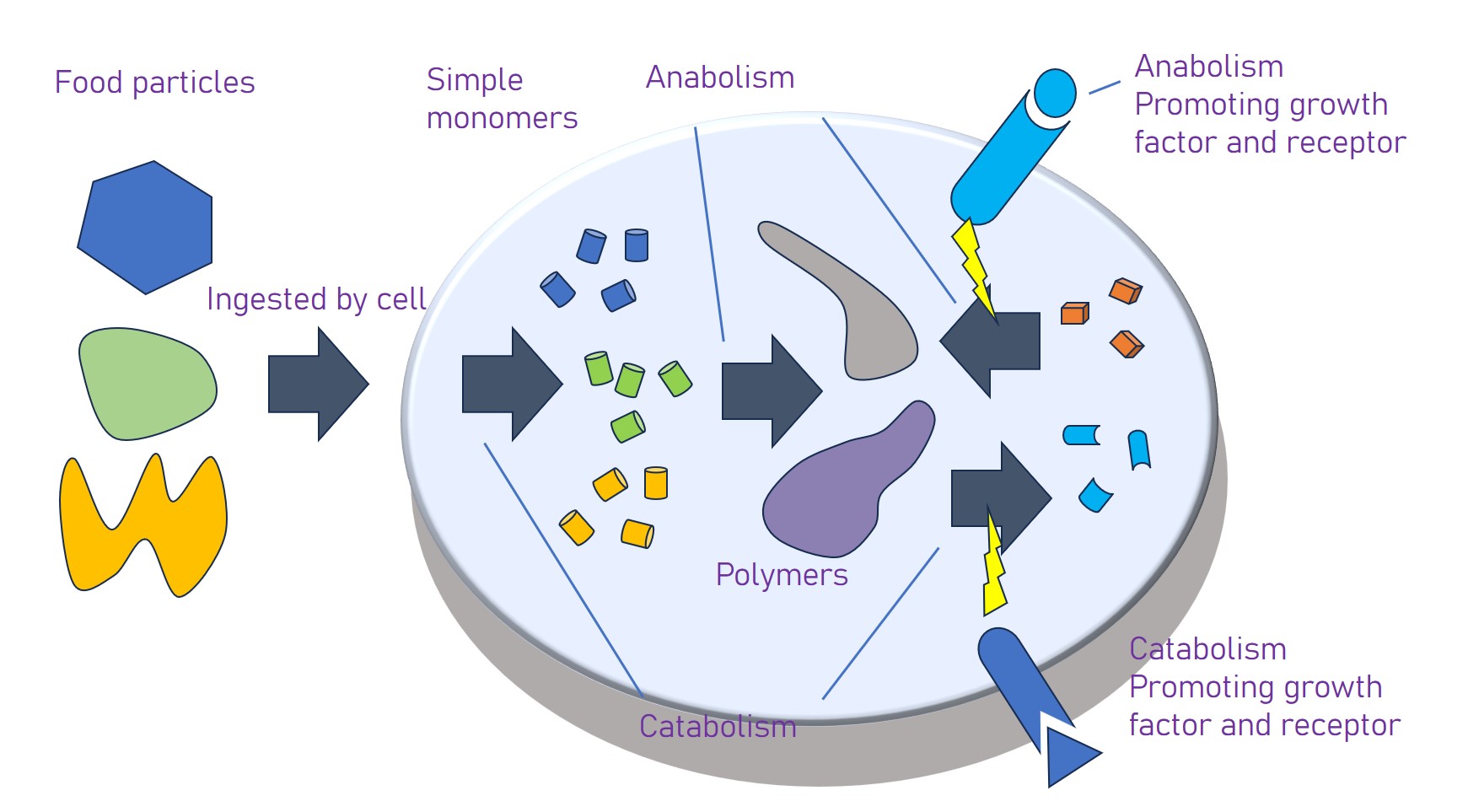
Le trasformazioni cellulari si organizzano secondo due direttrici complementari: vie cataboliche e vie anaboliche. Il catabolismo converte nutrienti complessi in molecole più semplici (per esempio, CO2, H2O, NH3, acetil-CoA e intermedi del ciclo degli acidi tricarbossilici), estraendo energia chimica e fornendo precursori per la biosintesi. L’anabolismo utilizza quell’energia e tali precursori per costruire i costituenti della cellula e le sue macromolecole. Le reazioni endoergoniche dell’anabolismo (\(\Delta G > 0\)) vengono rese possibili accoppiandole a processi esoergonici (\(\Delta G < 0\)) in modo che la somma risulti favorevole: \( \Delta G_{\text{tot}} = \Delta G_1 + \Delta G_2 < 0 \). L’accoppiamento è mediato da molecole trasduttrici di energia e potere riducente, quali ATP, NADH, NADPH e FADH2, e da gruppi ad alta energia (ad esempio i tioesteri dell’acetil-CoA). L’intero metabolismo può essere visto come l’integrazione dinamica di queste vie e dei relativi nodi di controllo (Figura 01.11-02).
La descrizione puntuale delle singole tappe enzimatiche appartiene alla biochimica. Ai fini della biologia cellulare, sono centrali alcuni principi generali: la necessità di un apporto continuo di energia dall’ambiente per contrastare la tendenza al disordine, il ruolo della catalisi enzimatica nell’abbassare le barriere cinetiche che limiterebbero le reazioni alle temperature fisiologiche, e l’impiego di specifici vettori chimici per immagazzinare, trasferire e distribuire energia e gruppi funzionali. In virtù di tali principi, le cellule costruiscono e mantengono ordine molecolare rispettando le leggi della termodinamica.