Nel ciclo cellulare la fase mitotica si alterna all’interfase
Definizione
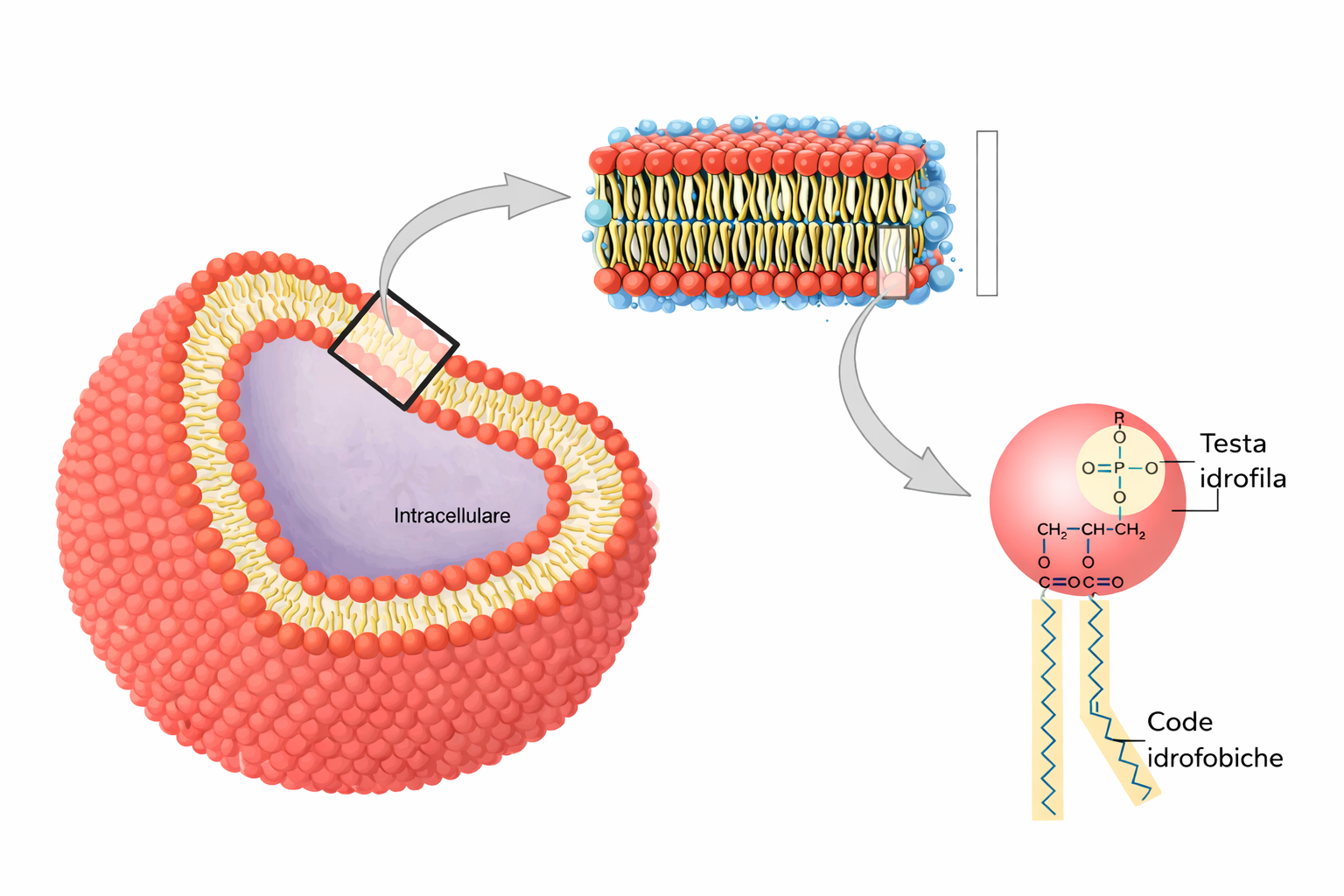
All’interno e all’esterno delle cellule sono presenti soluzioni acquose; di conseguenza, l’architettura delle membrane deriva direttamente dal modo in cui i lipidi si organizzano in acqua. I lipidi sono scarsamente solubili in acqua ma si estraggono agevolmente con solventi organici, come il benzene. Questa proprietà è stata decisiva nei primi studi strutturali: nel 1925, analizzando membrane di eritrociti (cellule prive di organuli che semplificano l’interpretazione), i ricercatori solubilizzarono i lipidi in benzene e li trasferirono come monostrato su una superficie acquosa, comprimendoli con una barriera mobile in un trogolo alla Langmuir. L’area del monostrato compresso risultò circa doppia rispetto alla superficie totale delle cellule di partenza. Da tale proporzione si dedusse che, nella membrana intatta, i lipidi sono disposti in due foglietti accoppiati, cioè in un doppio strato. Questa conclusione, poi confermata da molteplici approcci fisico‑chimici e microscopici, ha fondato la moderna visione delle membrane. Di seguito considereremo il doppio strato lipidico quale nucleo strutturale comune a tutte le membrane cellulari, illustrandone la formazione, la stabilità e le proprietà che conferiscono alle membrane le loro caratteristiche generali.
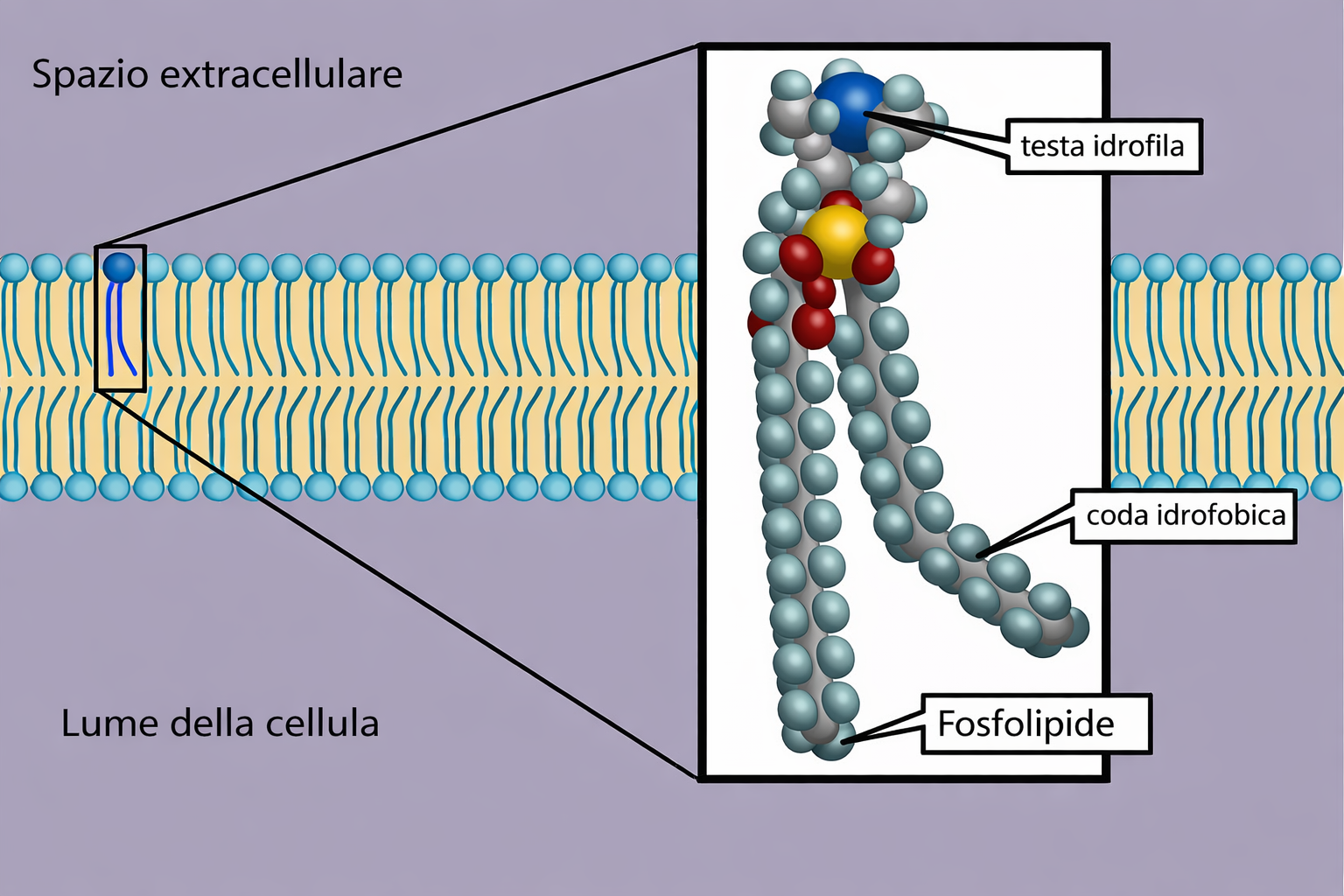
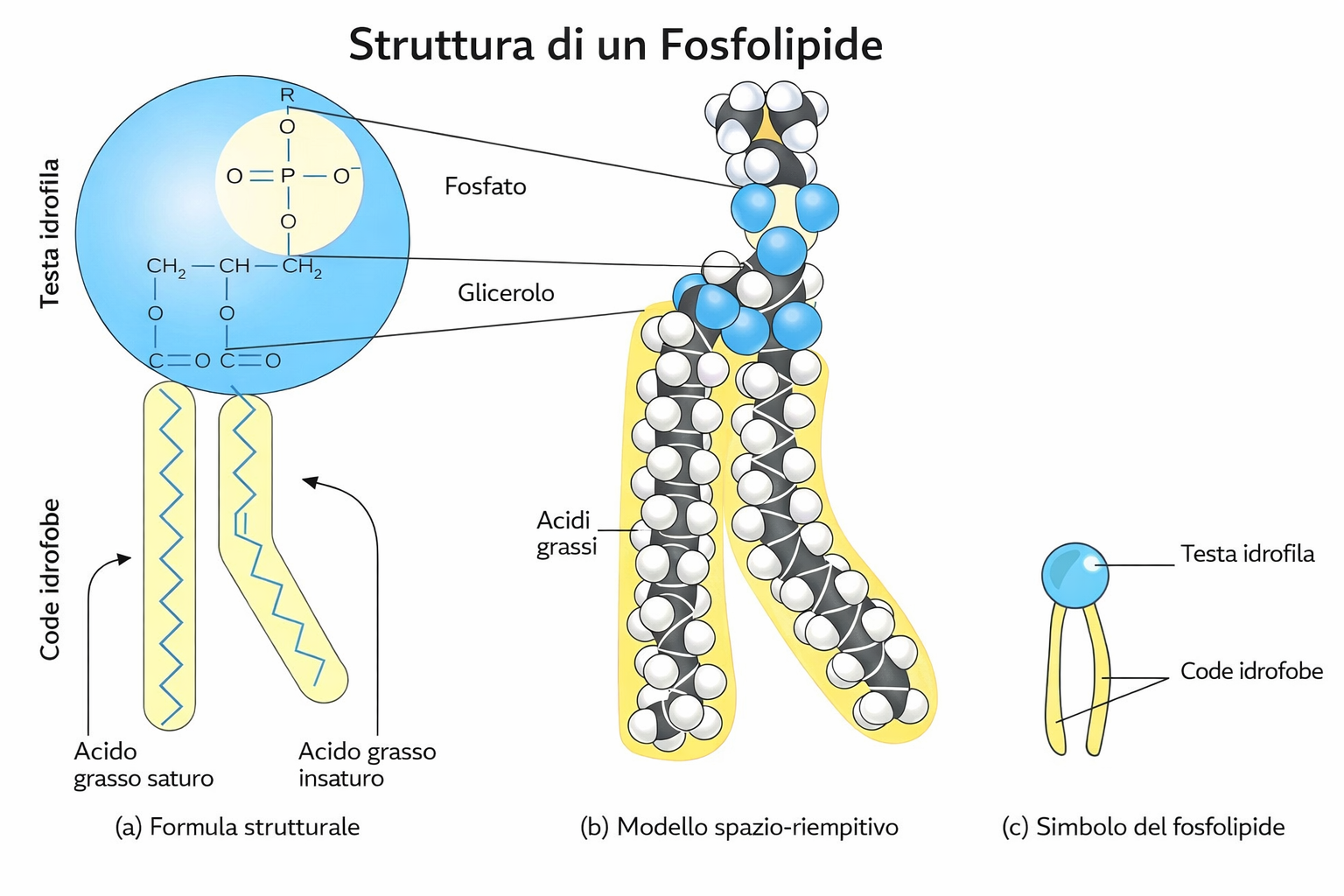
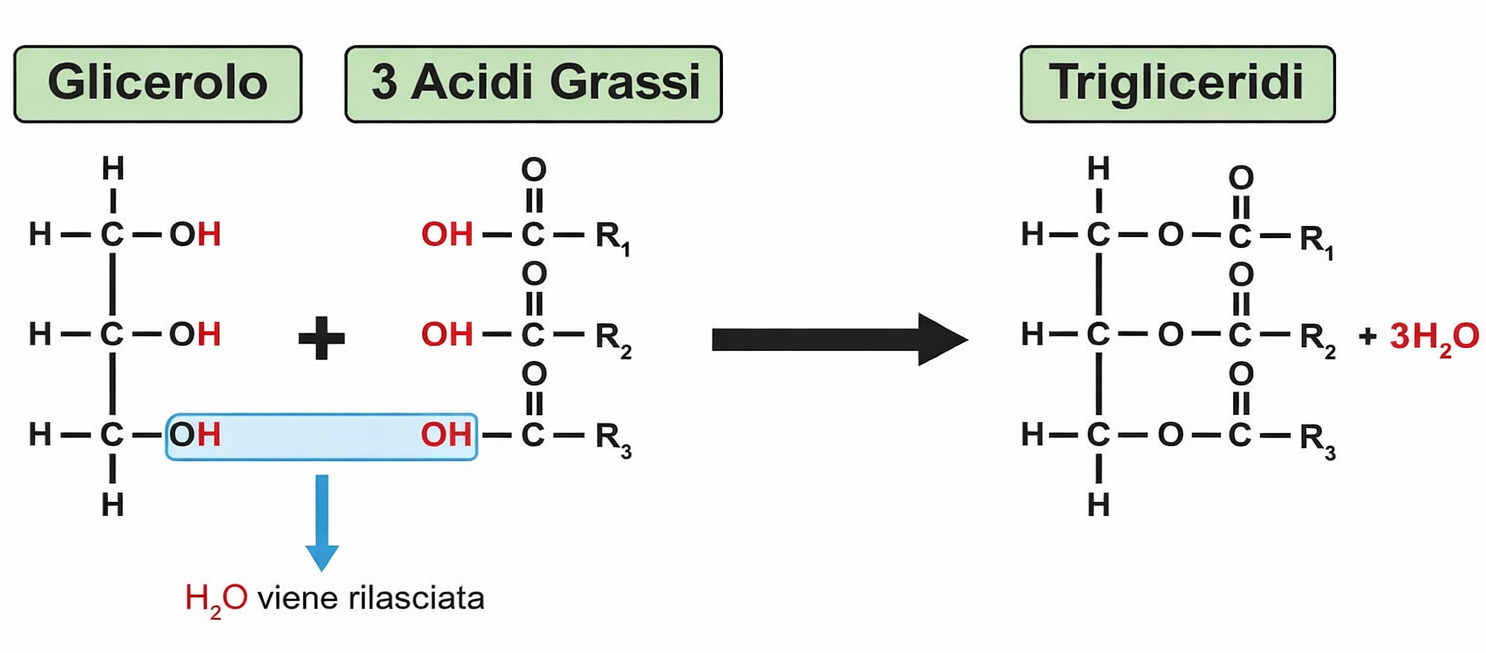
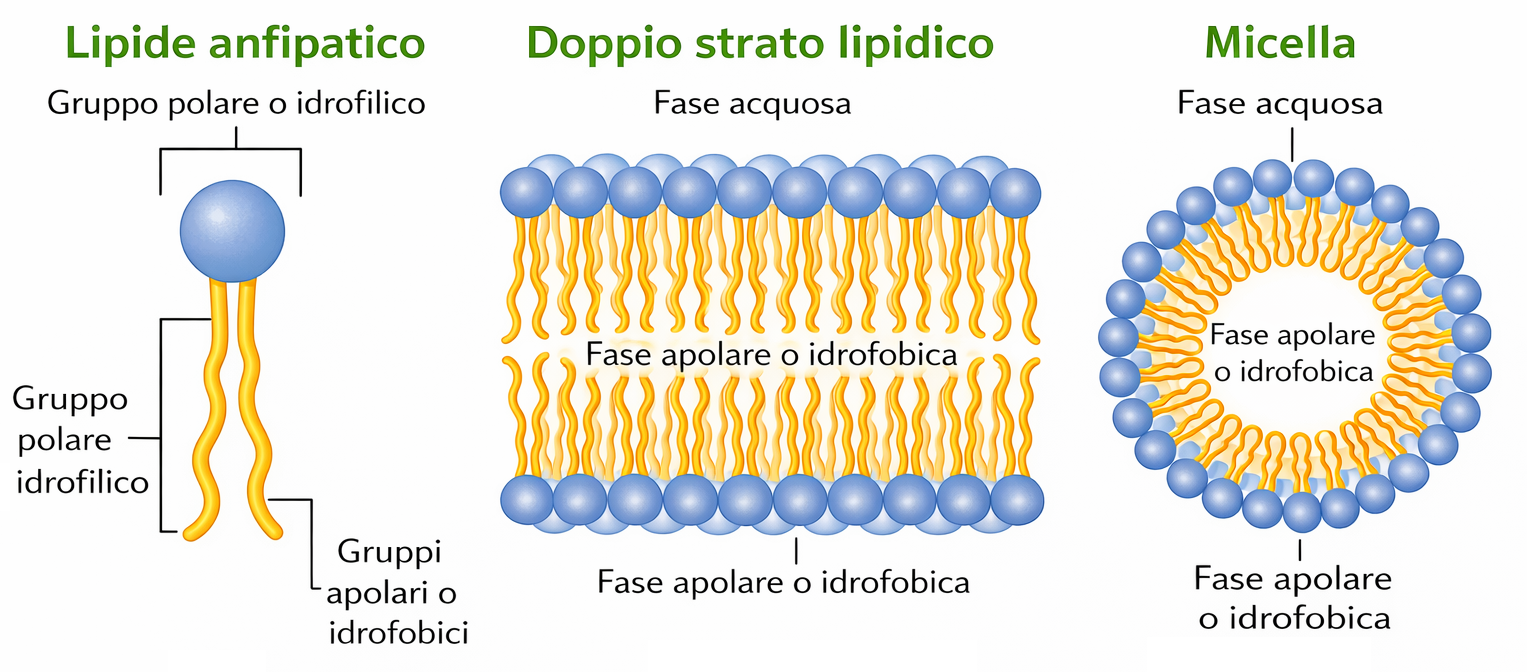
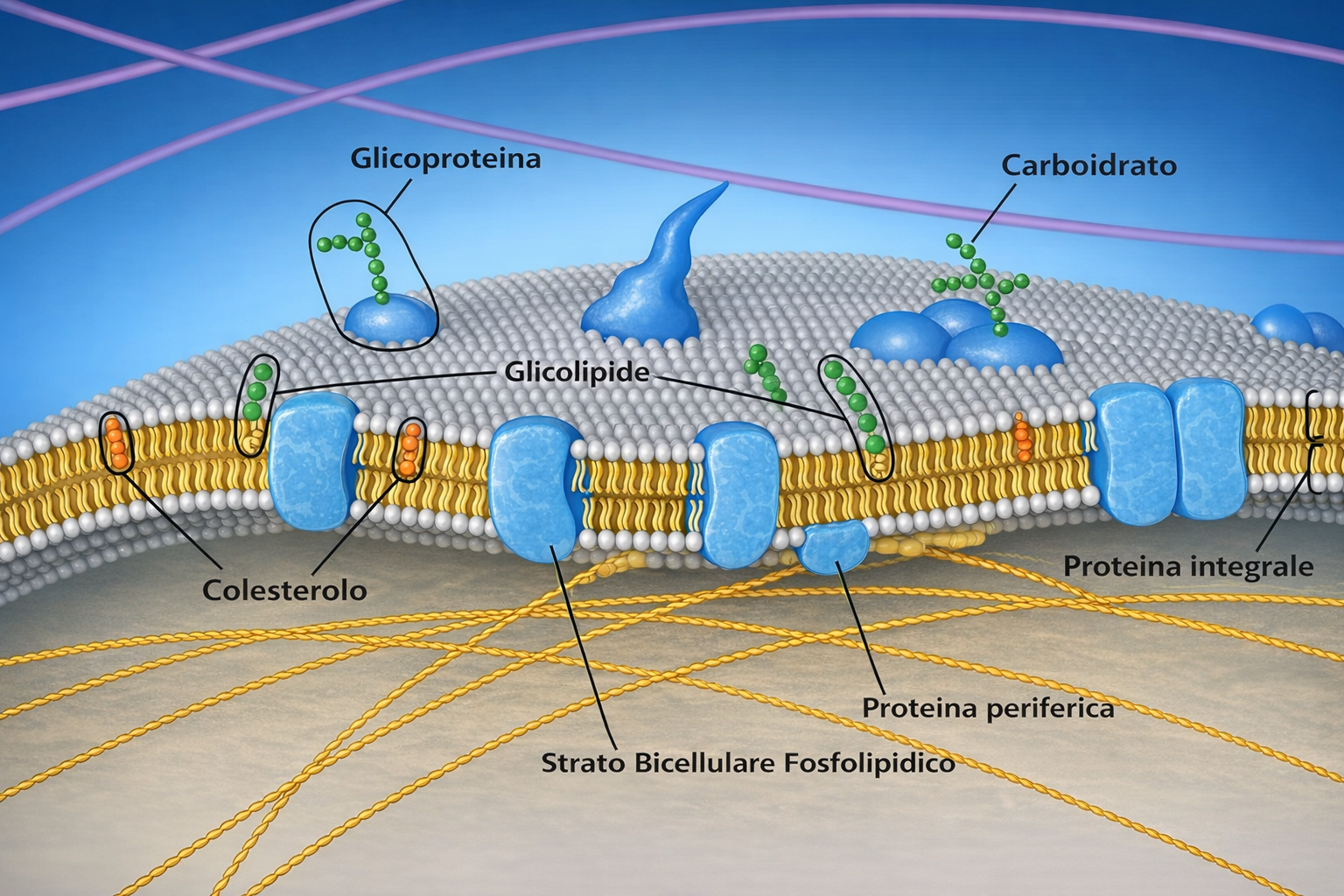
I lipidi di membrana sono molecole anfipatiche, caratterizzate dalla compresenza di una testa idrofila e di una o più code idrofobe. Tra essi predominano i fosfolipidi, nei quali un gruppo fosfato, parte della testa polare, è connesso a due catene idrocarburiche apolari (Figura 05.01-01). Un esempio tipico è la fosfatidilcolina, la cui testa idrofila include la colina legata al fosfato (Figura 05.01-02). Anche altre classi lipidiche di membrana sono anfipatiche: il colesterolo, abbondante nelle cellule animali, e i glicolipidi, che presentano teste polari costituite da mono- o oligosaccaridi (Figura 05.01-03).
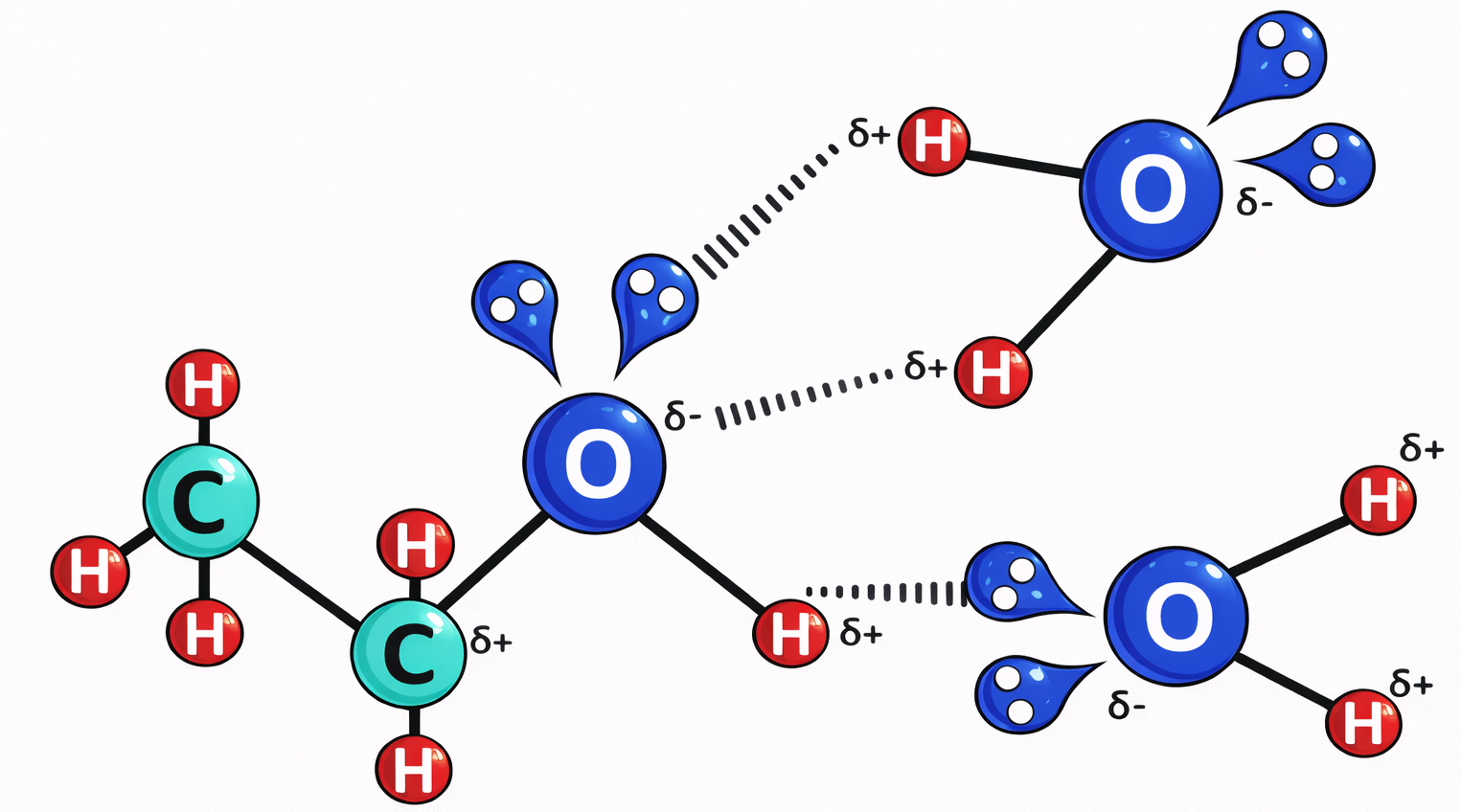
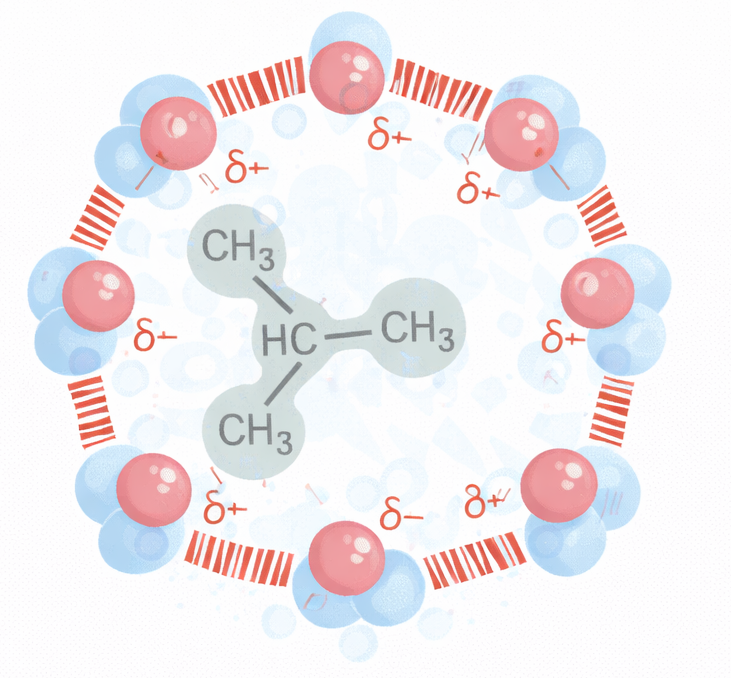
Le porzioni idrofile interagiscono favorevolmente con l’acqua attraverso gruppi carichi e polari capaci di formare attrazioni elettrostatiche e legami a idrogeno con le molecole del solvente (Figura 05.01-04). Al contrario, le parti idrofobe, costituite per lo più da atomi non polari, non stabiliscono interazioni favorevoli con l’acqua e inducono una riorganizzazione locale delle molecole d’acqua in strutture più ordinate, di tipo gabbia (Figura 05.01-05), con un costo entropico. La minimizzazione dell’energia libera del sistema spinge le regioni idrofobe ad aggregare tra loro, riducendo l’area di contatto con l’acqua; da ciò deriva, per esempio, la coalescenza dei grassi negli adipociti e degli oli nei semi in goccioline macroscopiche quando dispersi in acqua (Figura 05.01-06).
Per le molecole anfipatiche di membrana (Figura 05.01-03), la competizione tra la tendenza della testa a contattare l’acqua e quella delle code a evitare l’acqua si risolve in un’organizzazione in doppio strato: le teste idrofile si dispongono verso i due ambienti acquosi, mentre le code idrofobe si associano al centro, schermate dal solvente, analogamente alla farcitura racchiusa tra due fette (Figura 05.01-07). Il risultato è un assetto fortemente favorito dal punto di vista energetico. Una descrizione geometrico‑chimica utile è il parametro di impaccamento critico, \( \mathrm{CPP} = \frac{v}{a_0\, l} \), dove v è il volume della coda, \(a_0\) l’area della testa e l la lunghezza della coda: valori prossimi a 1 favoriscono i bilayer, mentre valori minori o maggiori tendono, rispettivamente, a micelle o fasi invertite.
Le stesse forze che portano alla formazione del doppio strato lo rendono anche autosigillante. La creazione di un bordo libero espone catene idrofobe all’acqua e comporta un costo energetico proporzionale alla lunghezza del bordo, che può essere schematizzato come \(E \approx \lambda\, L\), con \(\lambda\) tensione di linea e L lunghezza del margine. Perciò piccole discontinuità vengono eliminate spontaneamente grazie al riassestamento dei lipidi, mentre rotture estese possono indurre il ripiegamento del foglietto e la segmentazione in vescicole per sopprimere rapidamente l’esposizione idrofoba. La conseguenza più importante è che un foglietto anfipatico tende a chiudersi su se stesso, generando compartimenti chiusi privi di bordi esposti (Figura 05.01-08). Tale proprietà, all’origine della compartimentazione cellulare, scaturisce unicamente dalla duplice natura idrofila/idrofoba delle singole molecole.
L’ambiente acquoso su entrambi i lati della membrana impedisce ai lipidi di allontanarsi dal doppio strato, ma non ostacola il loro moto entro il piano del bilayer. La membrana si comporta quindi come un fluido bidimensionale, una caratteristica essenziale per funzione e integrità. Inoltre, il doppio strato è meccanicamente flessibile e può curvarsi; questa proprietà, insieme alle caratteristiche elastiche della membrana, pone un limite inferiore realistico al diametro delle vescicole cellulari, tipicamente non inferiore a circa 25 nm.
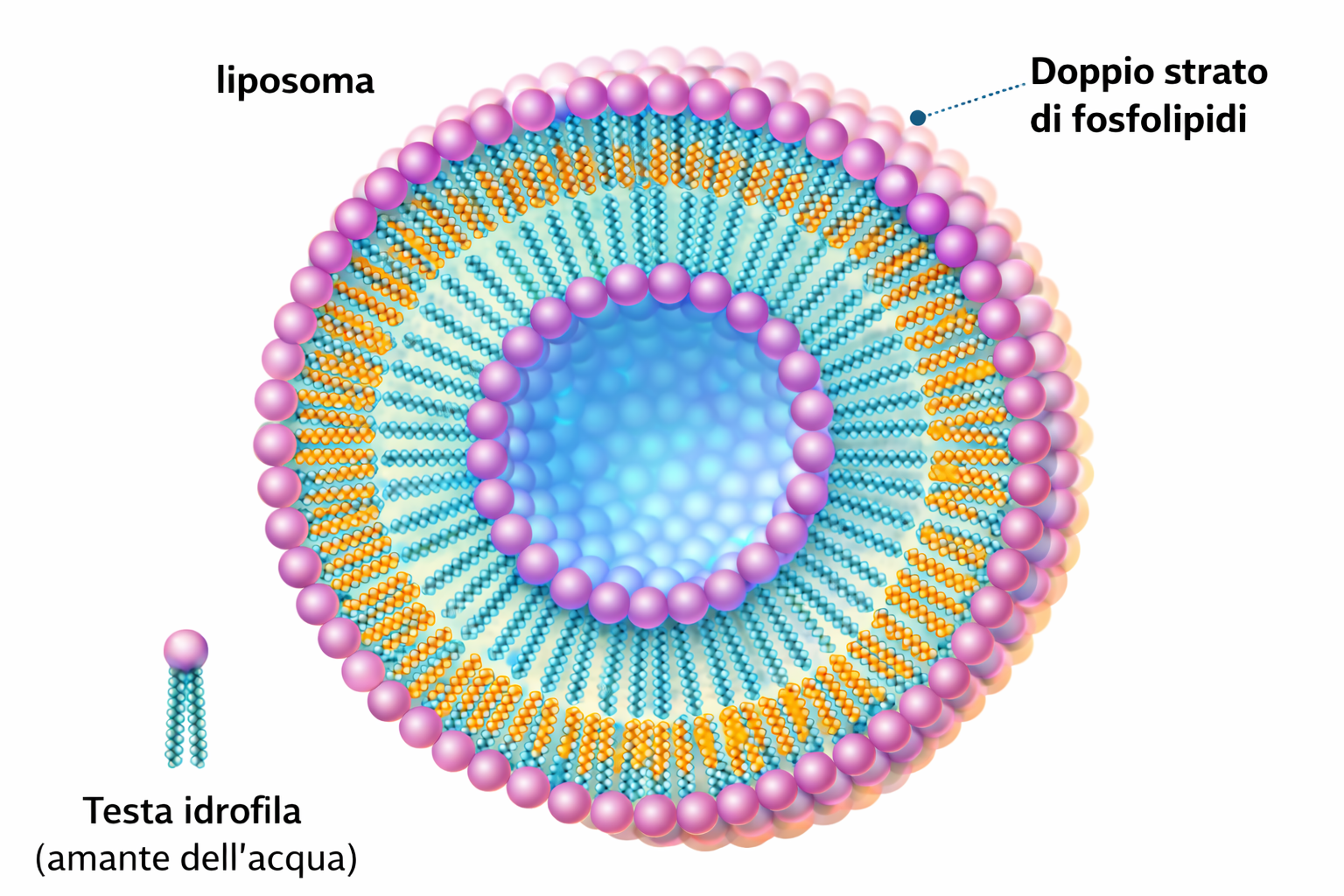
La fluidità può essere studiata in sistemi artificiali ottenuti per auto‑assemblaggio di lipidi anfipatici in acqua. L’aggiunta di fosfolipidi purificati genera vescicole sferiche chiuse (liposomi) con diametri che vanno da circa 25 nm fino a 1 mm, in funzione delle condizioni di formazione (Figura 05.01-09). Questi modelli permettono di quantificare le diverse modalità di movimento dei lipidi: alcune sono rare, altre estremamente frequenti.
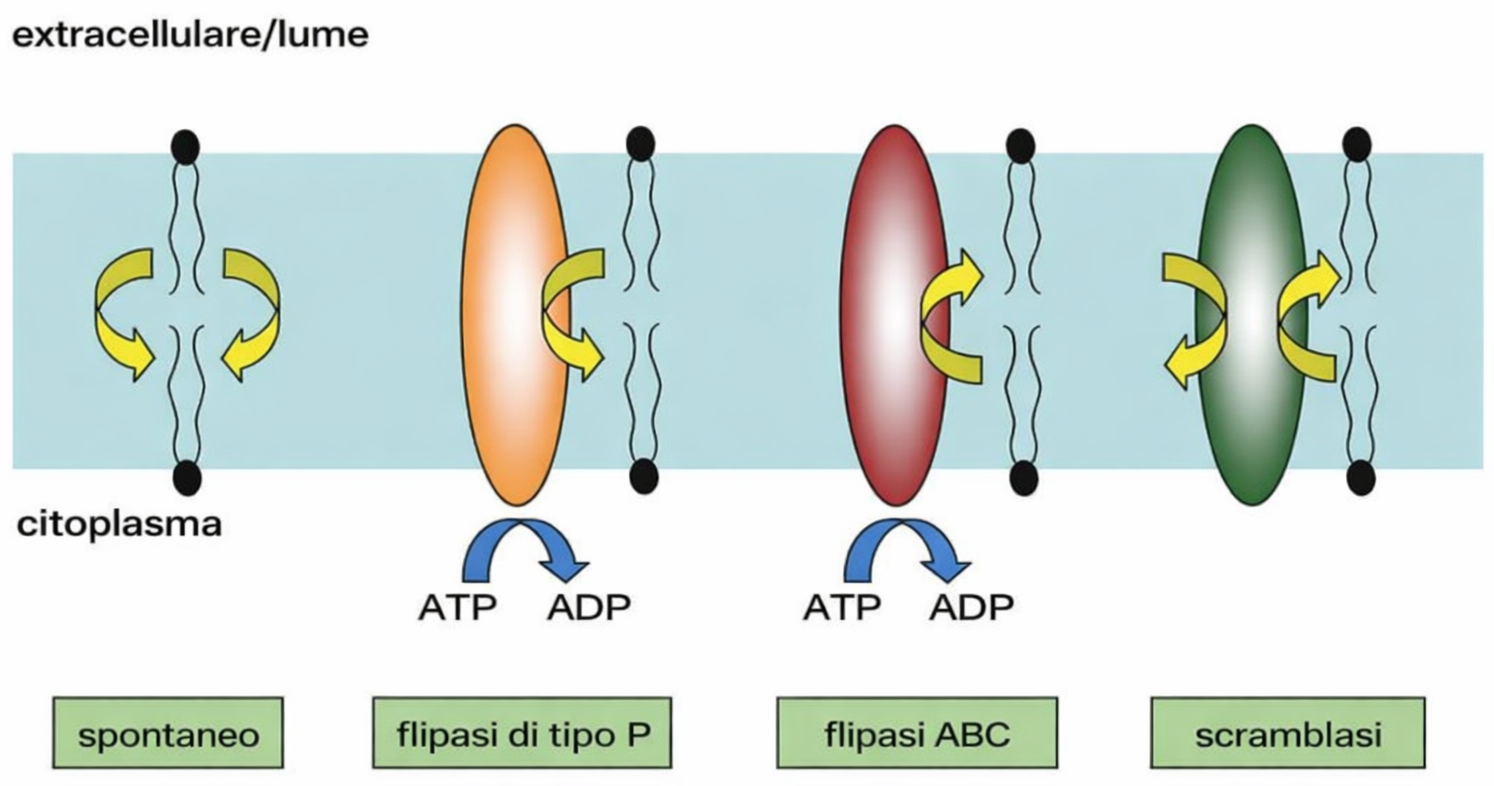
In condizioni fisiologiche, il passaggio di una molecola lipidica da un foglietto all’altro (flip‑flop) avviene con estrema lentezza in assenza di proteine che catalizzino il processo (come scramblasi e flippasi), su scale temporali dell’ordine di molte settimane per singola molecola. Al contrario, i lipidi si spostano rapidamente lateralmente entro lo stesso foglietto per diffusione termica. In un doppio strato artificiale, una molecola può coprire distanze dell’ordine di micrometri in circa un secondo; ad esempio, spostarsi di 1,7 μm, comparabile alle dimensioni longitudinali di una cellula batterica. Le singole molecole, inoltre, possono flettere le code idrocarburiche e ruotare attorno al proprio asse lungo a velocità molto elevate, con frequenze che possono raggiungere centinaia di giri al secondo.
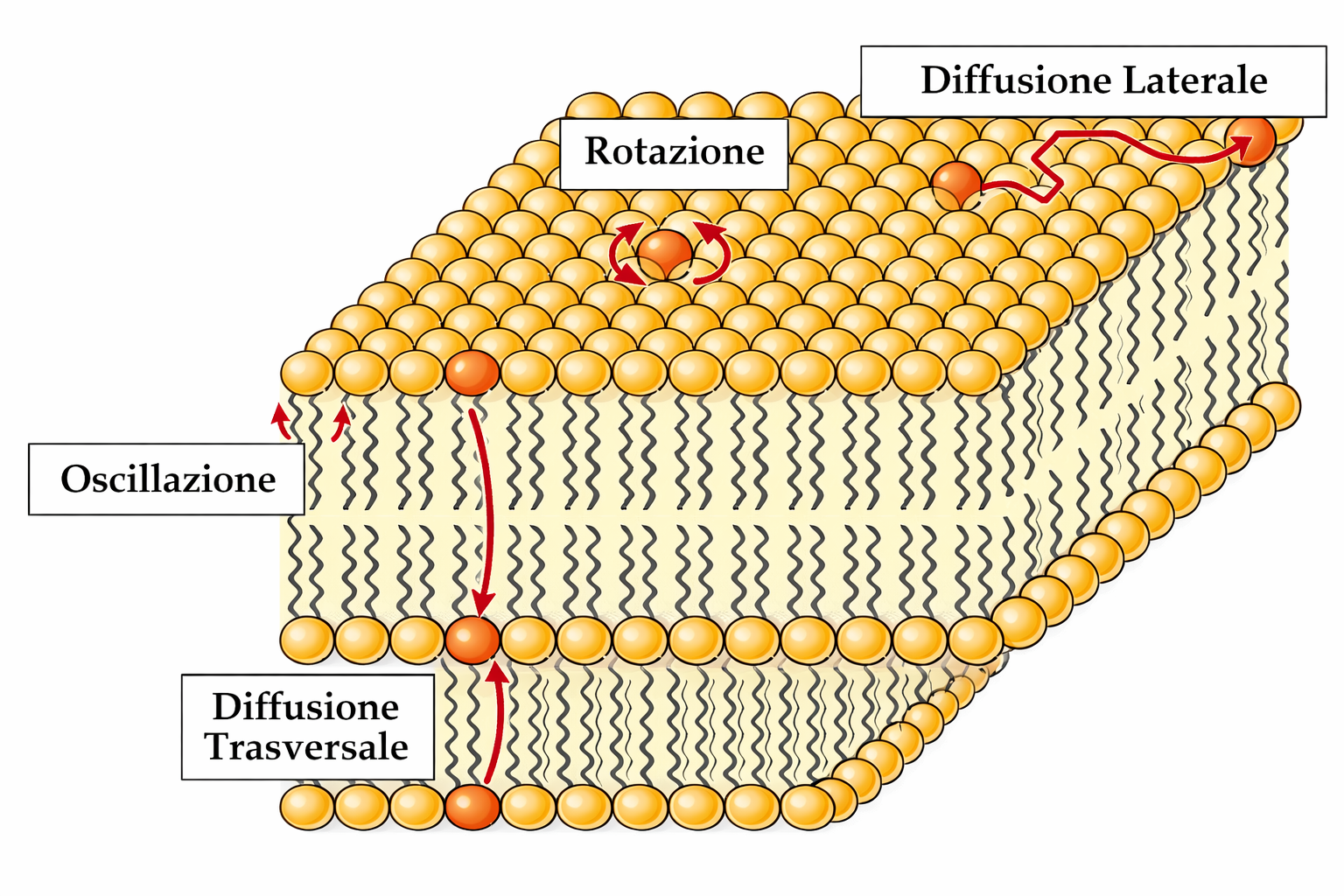
Le osservazioni su membrane cellulari isolate e su cellule integre confermano che i lipidi biologici presentano gli stessi schemi dinamici individuati nei bilayer artificiali. I principali tipi di movimento dei fosfolipidi sono riassunti nella (Figura 05.01-10) e comprendono:
- diffusione laterale rapida entro il monostrato con scambi frequenti di posizione con le molecole adiacenti;
- rotazione intorno all’asse maggiore della molecola;
- flessione conformazionale delle code idrocarburiche;
- flip‑flop tra i due foglietti, evento rarissimo in assenza di catalisi proteica.
Per fluidità di membrana si intende la rapidità con cui i lipidi si spostano lateralmente all’interno del piano del doppio strato. Tale proprietà, essenziale per la funzione biologica delle membrane, deve restare entro intervalli ristretti a una data temperatura. La fluidità dipende in larga misura dall’identità chimica dei fosfolipidi e, in particolare, dalle caratteristiche delle code idrocarburiche: quanto più le catene interagiscono strettamente e si impacchettano con regolarità, tanto maggiore è la viscosità, e dunque minore la fluidità del doppio strato.
Due parametri strutturali delle code idrocarburiche determinano l’entità delle interazioni tra catene adiacenti: la lunghezza e il grado di insaturazione. Catene più corte presentano minori superfici di contatto e forze di van der Waals ridotte, favorendo una maggiore mobilità laterale. Nelle membrane biologiche le code variano tipicamente da 14 a 24 atomi di carbonio, con un’abbondanza di catene di 18–20 atomi. In molti fosfolipidi una delle due code contiene uno o più doppi legami, mentre l’altra è totalmente satura (Figura 05.01-02). La presenza di doppi legami, in genere in configurazione cis, introduce pieghe (“gomiti”) nello scheletro carbonioso, riducendo l’impacchettamento tra catene adiacenti e accrescendo la fluidità; al contrario, catene lunghe e sature promuovono un’organizzazione più ordinata e meno mobile del doppio strato.
Una coda priva di doppi legami è definita satura poiché contiene il numero massimo di atomi di idrogeno consentito dalla struttura carboniosa; una coda con doppi legami è detta insatura, poiché meno ricca di idrogeno. I “gomiti” generati dai doppi legami (Figura 05.01-02) ostacolano l’allineamento regolare delle catene, spiegando perché membrane ricche di code insature manifestino una fluidità superiore rispetto a membrane in cui predominano code sature. Questo comportamento si riflette nella temperatura di transizione termica della membrana, spesso indicata come Tm: catene più lunghe e più sature innalzano la Tm, mentre catene più corte e insature la abbassano.
Molti microrganismi regolano la composizione delle loro membrane per mantenere stabile la fluidità al variare della temperatura, un fenomeno noto come adattamento omeoviscoso. In batteri e lieviti si osservano aggiustamenti coordinati della lunghezza delle catene e del grado di insaturazione: a temperature elevate prevalgono lipidi con catene più lunghe e meno doppi legami; a temperature ridotte, al contrario, aumentano i doppi legami e si accorciano le catene, così da evitare l’eccessiva rigidità. Un’analoga logica chimica sta alla base del trattamento industriale degli oli vegetali: l’idrogenazione riduce i doppi legami rendendo più consistenti gli oli a temperatura ambiente; per esempio, la produzione di grassi “shortening” per prodotti da forno sfrutta l’addizione di idrogeno per ottenere una consistenza solida a temperatura ambiente, paragonabile a quella dei grassi animali.
Nelle cellule animali, la fluidità è modulata anche dagli steroli, in particolare dal colesterolo, che può costituire circa il 20% in peso dei lipidi della membrana plasmatica. Le molecole di colesterolo, corte e rigide, si intercalano tra le code dei fosfolipidi, riempiendo i microspazi creati dai gomiti delle catene insature (Figura 05.01-11). Questo effetto riduce la permeabilità ai piccoli soluti e smorza le fluttuazioni di fluidità: a temperature alte limita il movimento eccessivo delle catene, mentre a basse temperature ostacola la cristallizzazione del doppio strato. Insieme a sfingolipidi a lunga catena e relativamente saturi, il colesterolo può favorire stati “liquido-ordinati” rispetto a regioni più “liquido-disordinate”, contribuendo alla compartimentazione laterale della membrana.
La fluidità controllata del doppio strato ha ricadute funzionali cruciali:
- permette alle proteine integrali di diffondere nel piano della membrana e di formare complessi transitori, evento determinante per processi come la trasduzione del segnale e l’adesione cellulare;
- consente a lipidi e proteine di spostarsi dal sito di inserzione verso altre microdomini o membrane, facilitando il traffico intra- e inter-compartimentale;
- rende possibile la fusione tra membrane e la successiva rimescolanza dei componenti, essenziale per esocitosi, endocitosi e traffico vescicolare;
- assicura una corretta ripartizione della membrana tra cellule figlie durante la divisione, prevenendo asimmetrie dannose.
Nelle cellule eucariotiche la biosintesi dei fosfolipidi avviene su enzimi collocati sulla faccia citosolica del reticolo endoplasmatico (RE). Utilizzando acidi grassi attivati e glicerolo-3-fosfato, tali enzimi formano prima acido fosfatidico e, successivamente, i diversi fosfolipidi, che vengono inseriti nel foglietto citoplasmatico del doppio strato dell’RE. Questo porta a una crescita inizialmente sbilanciata della membrana, limitata a un solo foglietto.
Poiché il “flip-flop” spontaneo dei fosfolipidi tra i due foglietti è energeticamente sfavorevole e rarissimo a scala temporale cellulare (Figura 05.01-10), l’equilibrio tra i foglietti è ristabilito da proteine di traslocazione bidirezionale, dette scramblasi. Queste proteine catalizzano lo scambio non selettivo di fosfolipidi tra i due strati, ottenendo una ripartizione pressoché equa dei lipidi recentemente sintetizzati (Figura 05.01-12). In tal modo, la membrana dell’RE cresce in modo omogeneo nonostante l’assemblaggio abbia luogo sul solo lato citoplasmatico.
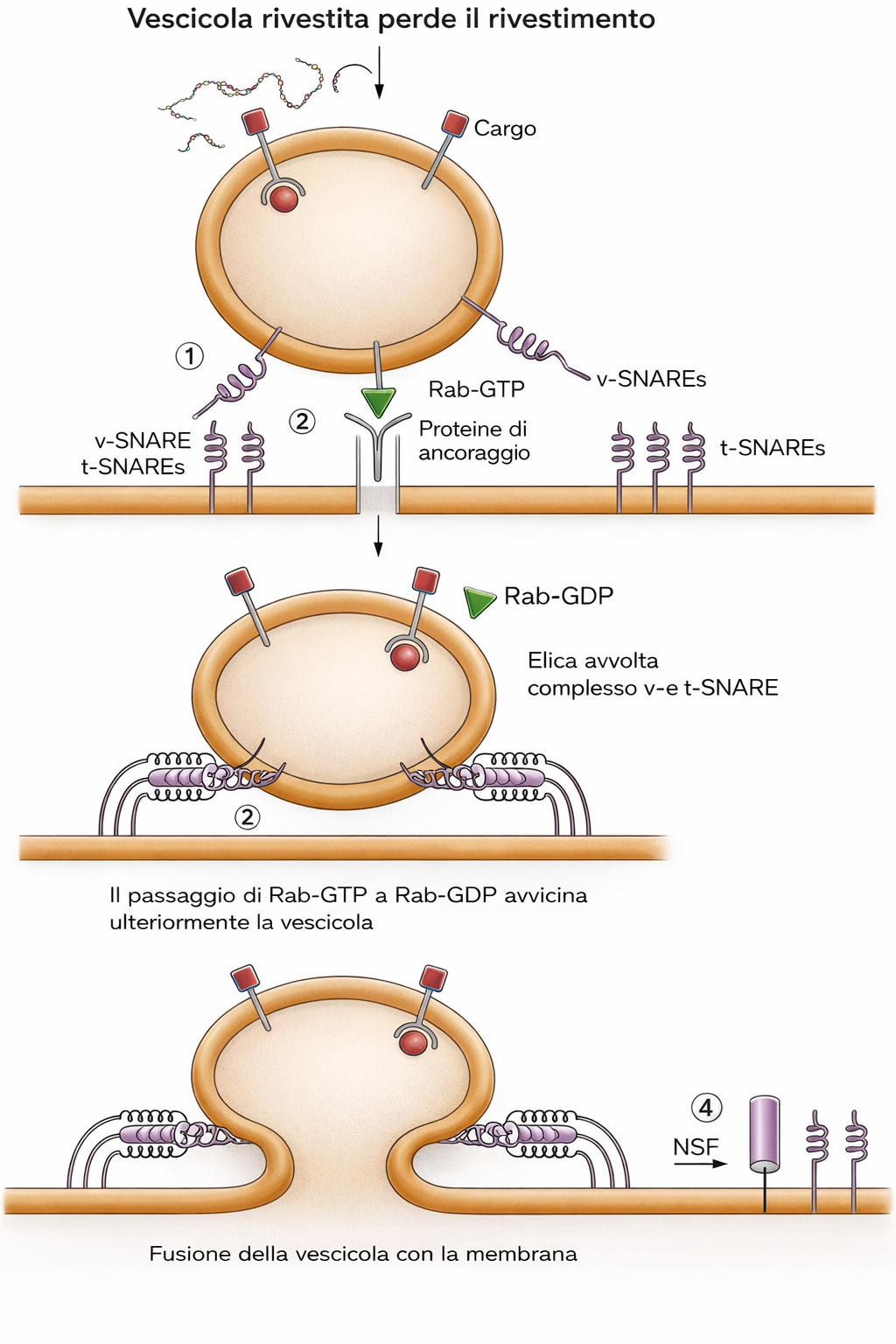
Porzioni di membrana neoformata restano a costituire l’RE, mentre altre sono trasferite ad ulteriori compartimenti, in particolare all’apparato di Golgi e, attraverso la via secretoria, alla membrana plasmatica. Dall’RE gemmano continuamente vescicole rivestite che si fondono con compartimenti intermedi e con il Golgi; a loro volta, dal Golgi originano vescicole dirette alla superficie cellulare. Durante l’intero percorso, l’orientamento topologico dei doppi strati si mantiene: ciò che è rivolto verso il lume di RE e Golgi corrisponderà al lato non citoplasmatico quando la vescicola si fonderà con la membrana cellulare.
La membrana plasmatica è intrinsecamente asimmetrica: i due foglietti del doppio strato possiedono composizioni lipidiche differenti e funzioni distinte. Se dall’RE i fosfolipidi emergono grossomodo equilibrati grazie all’azione delle scramblasi, dove si genera l’asimmetria? Il rimodellamento ha luogo soprattutto nell’apparato di Golgi, in cui operano enzimi di trasporto direzionale, le flippasi. A differenza delle scramblasi, le flippasi spostano in modo selettivo specifiche specie lipidiche dal foglietto esposto verso il lume (destinato all’esterno) a quello rivolto verso il citoplasma, stabilendo una distribuzione non casuale (Figura 05.01-13). Enzimi affini con direzionalità opposta, spesso detti floppasi, esportano selettivamente lipidi dal foglietto citoplasmatico a quello luminale. L’azione coordinata di queste attività mantiene l’asimmetria lungo l’intera via secretoria.
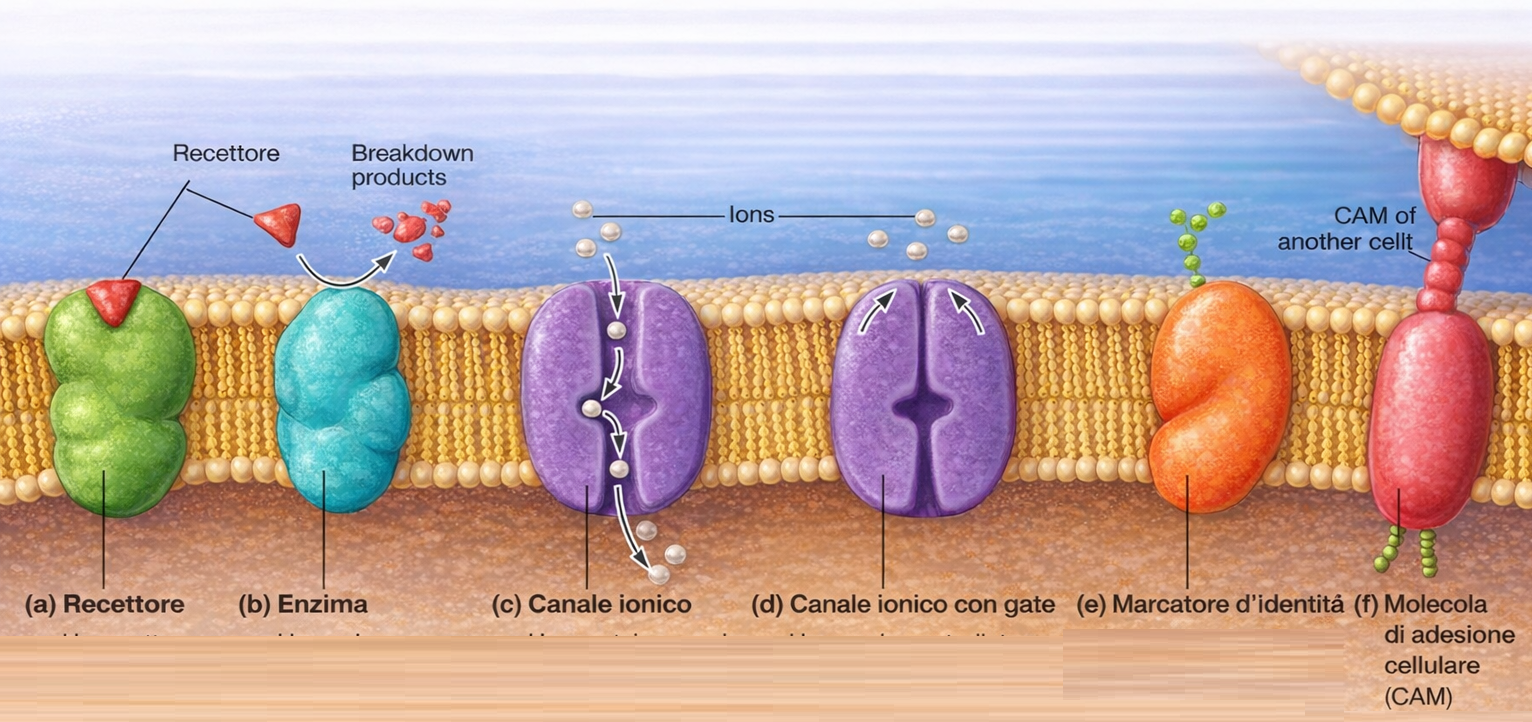
La conseguenza è una membrana con due facce riconoscibili: il foglietto citoplasmatico, costantemente rivolto verso il citosol, e il foglietto non citoplasmatico, esposto all’ambiente extracellulare o al lume degli organuli. Questa identità viene conservata durante il traffico vescicolare e riguarda sia i lipidi sia le proteine di membrana, che mantengono sul lato non citoplasmatico i domini luminali e su quello citosolico i domini citoplasmatici (Figura 05.01-14). Tale organizzazione è essenziale per la funzione, come è evidente per recettori, trasportatori e canali ionici, la cui attività dipende dall’orientamento dei domini funzionali (Figura 05.01-16).
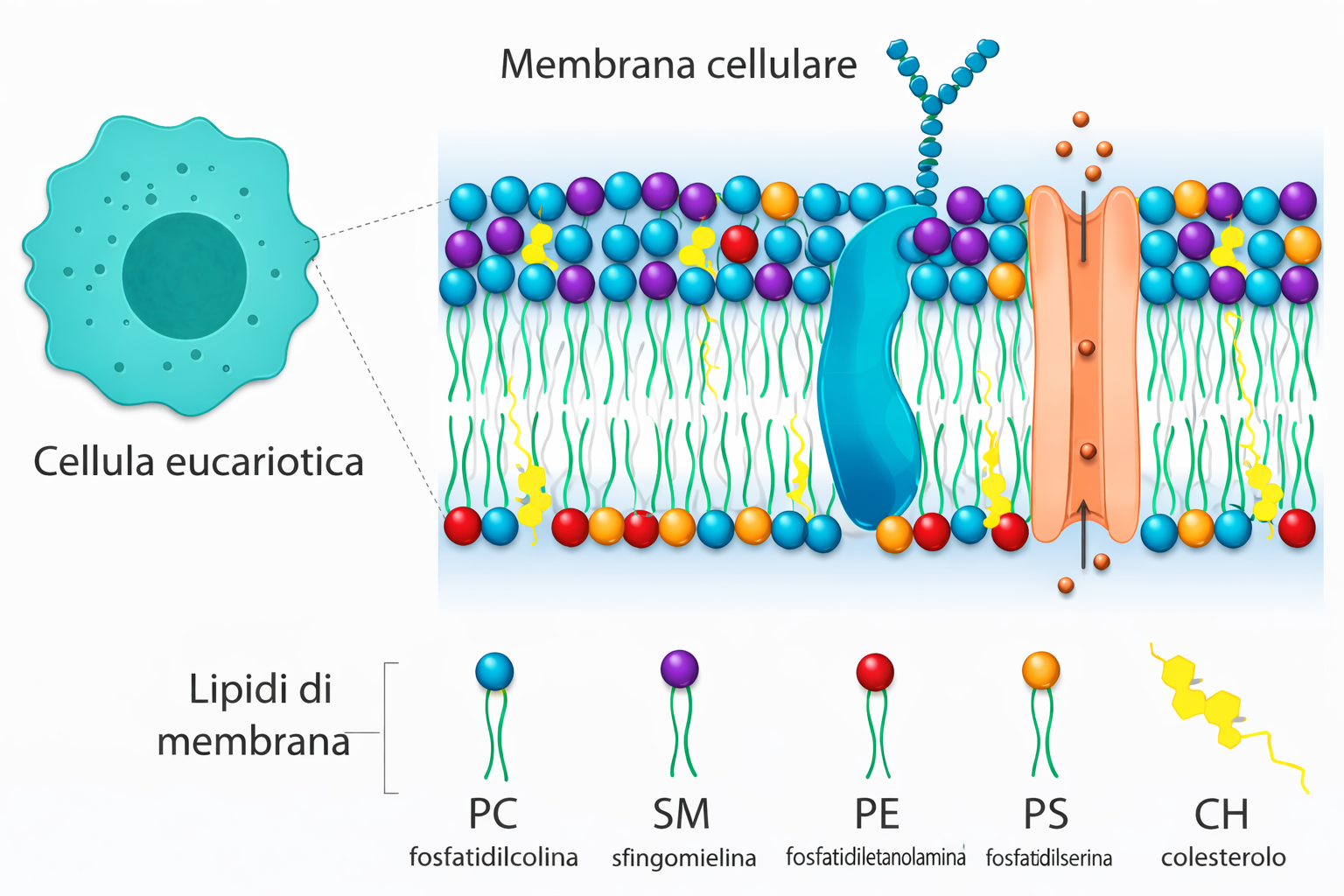
Un caso emblematico di distribuzione marcatamente asimmetrica è quello dei glicolipidi, localizzati prevalentemente nel foglietto esterno della membrana plasmatica (Figura 05.01-15). Le catene oligosaccaridiche dei glicolipidi, insieme a quelle di glicoproteine e proteoglicani, formano il rivestimento glucidico superficiale, che contribuisce alla protezione meccanica e chimica, al riconoscimento cellula-cellula e all’interazione con patogeni o molecole segnale. I residui glucidici sono aggiunti nell’apparato di Golgi da glicosiltransferasi orientate in modo che la glicosilazione avvenga sulle testine lipidiche esposte al lume; poiché non esistono flippasi che trasferiscano glicolipidi al foglietto opposto, le molecole glicosilate restano confinate sul lato non citoplasmatico fino all’arrivo alla membrana cellulare, dove le porzioni glucidiche sono esposte all’esterno.
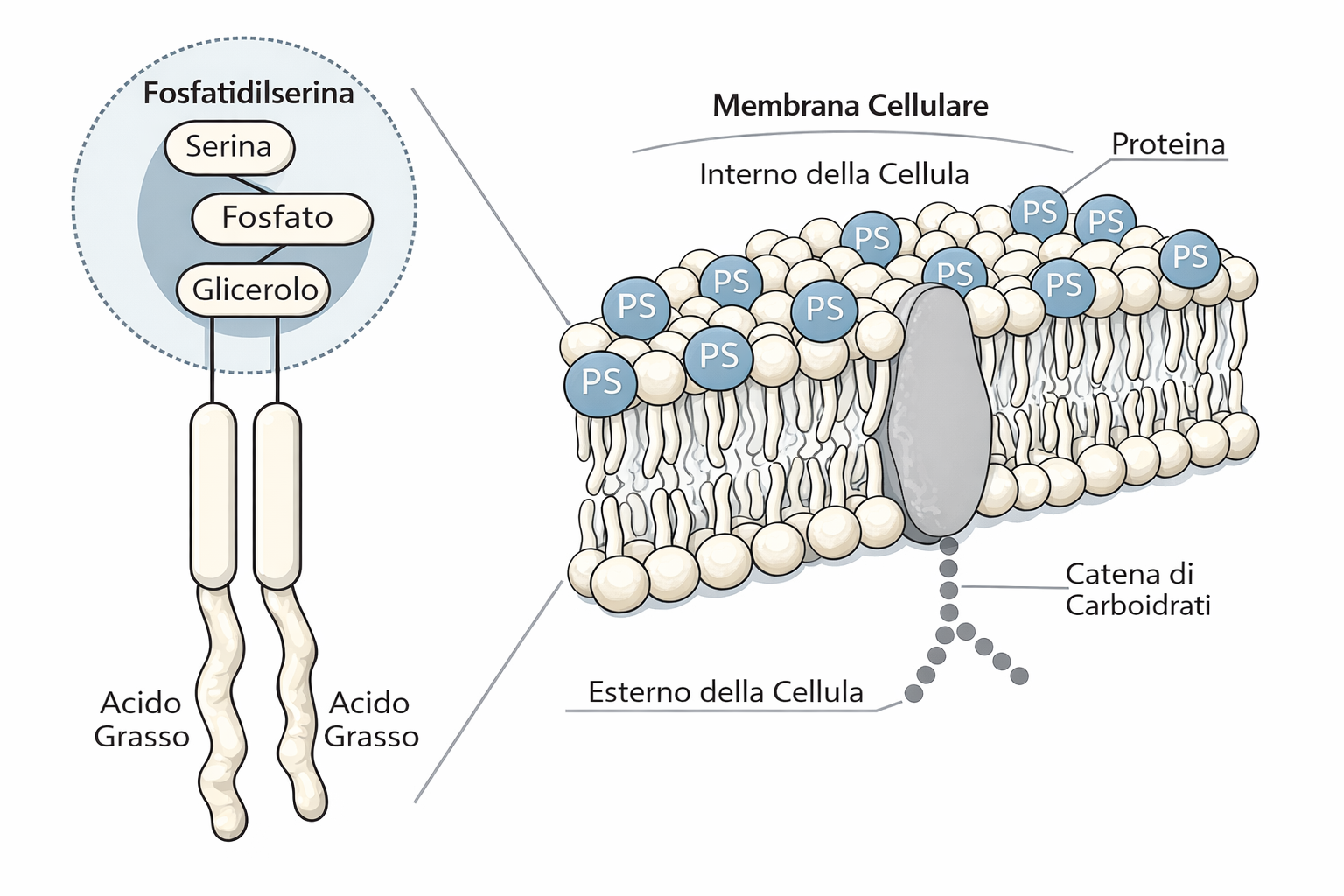
Altri fosfolipidi mostrano asimmetrie funzionalmente rilevanti. Fosfatidilserina (PS) e fosfatidiletanolamina (PE) sono in genere arricchite nel foglietto citoplasmatico, contribuendo alla carica negativa della superficie interna e al reclutamento di proteine citosoliche sensibili ai lipidi anionici; fosfatidilcolina (PC) e sfingomielina tendono a prevalere nel foglietto esterno. I fosfoinositidi, sebbene presenti in quantità minori, svolgono un ruolo centrale nella segnalazione: in prevalenza confinati nel foglietto citoplasmatico, fungono da piattaforme per domini di legame come PH e C2 e sono substrati per chinasi e fosfolipasi che attivano vie di segnale dirette dall’esterno verso l’interno della cellula. L’asimmetria non è statica: può essere rimodellata in risposta a stimoli, pur restando rigorosamente controllata per preservare le funzioni cellulari.
Complessivamente, la distribuzione asimmetrica dei lipidi sostiene una serie di processi:
- creazione di microambienti con proprietà fisico-chimiche diverse sui due lati della membrana, utili per trasporto e segnalazione;
- impianto corretto dell’orientamento delle proteine di membrana, da cui dipendono siti di legame, catalisi ed esposizione di epitopi;
- formazione del glicocalice, barriera protettiva e piattaforma per il riconoscimento specifico;
- modulazione della curvatura e della meccanica di membrana, facilitando gemmazione e fusione vescicolare.