Virus e prioni rappresentano pericolosi agenti patogeni per animali e piante
Definizione
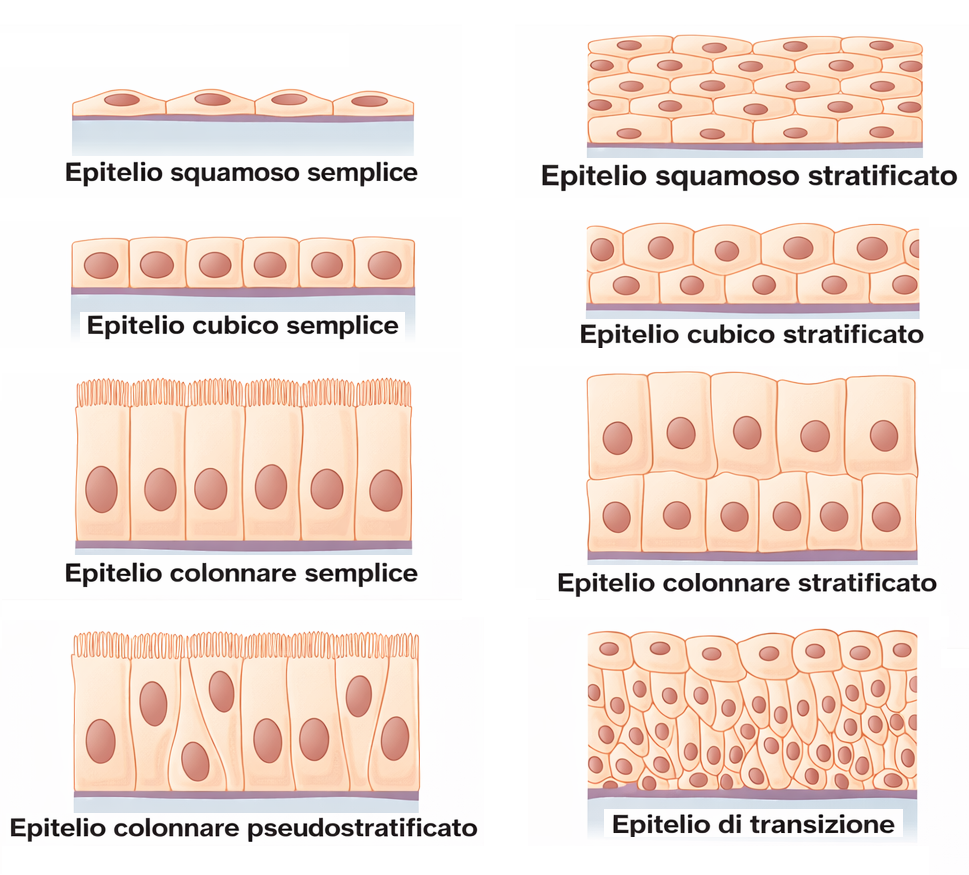
Nel corpo dei vertebrati si riconoscono oltre duecento tipologie cellulari distinte per morfologia e specializzazione funzionale. Una quota sostanziale di queste cellule è organizzata in epiteli, insiemi compatti in cui gli elementi cellulari si affiancano e costituiscono foglietti pluricellulari continui. La disposizione può essere semplice, quando lo strato è formato da un’unica fila di cellule, come nel rivestimento del tenue, oppure pluristratificata, quando più strati sovrapposti proteggono i tessuti sottostanti, come nell’epidermide. La forma delle cellule epiteliali varia da cilindrica ad altezza elevata a cubica, fino a un profilo appiattito di tipo pavimentoso (Figura 06.03-01). In un medesimo epitelio possono coesistere cellule omogenee o elementi di natura diversa, combinati per ottenere specifiche prestazioni fisiologiche. Gli epiteli rappresentano un’architettura modulare capace di sostenere funzioni molteplici: barriera meccanica e chimica, secrezione, assorbimento, e trasduzione di segnali. Esempi includono l’emissione di prodotti ghiandolari quali ormoni, latte o lacrime; l’assorbimento selettivo di nutrienti nel tubo digerente; la rilevazione di stimoli fisici, come l’energia luminosa da parte dei fotorecettori retinici o le vibrazioni sonore tramite le cellule capellute della coclea. A dispetto della grande eterogeneità, gli epiteli condividono un insieme di tratti strutturali ricorrenti: stretti contatti intercellulari, polarità apico-basale, interazione obbligata con una matrice di supporto e un’organizzazione citoscheletrica coordinata. Dal punto di vista istologico, molti epiteli sono avascolari e dipendono dalla diffusione attraverso la lamina basale per l’apporto di ossigeno e nutrienti; mostrano un ricambio dinamico grazie a compartimenti di cellule staminali; presentano specializzazioni di superficie, come microvilli, stereociglia o ciglia motili, funzionali a potenziare assorbimento, secrezione o movimentazione del fluido. L’evidenza comparativa suggerisce che l’assetto epiteliale si sia affermato precocemente nell’evoluzione animale: il foglietto epiteliale, come una membrana cellulare “a scala di tessuto”, delimita domini, regola il traffico di molecole, protegge da patogeni e limita la perdita di acqua e soluti. Tale risultato, apparentemente semplice, richiede un apparato integrato di giunzioni, recettori di adesione e complessi molecolari di polarità finemente regolati.
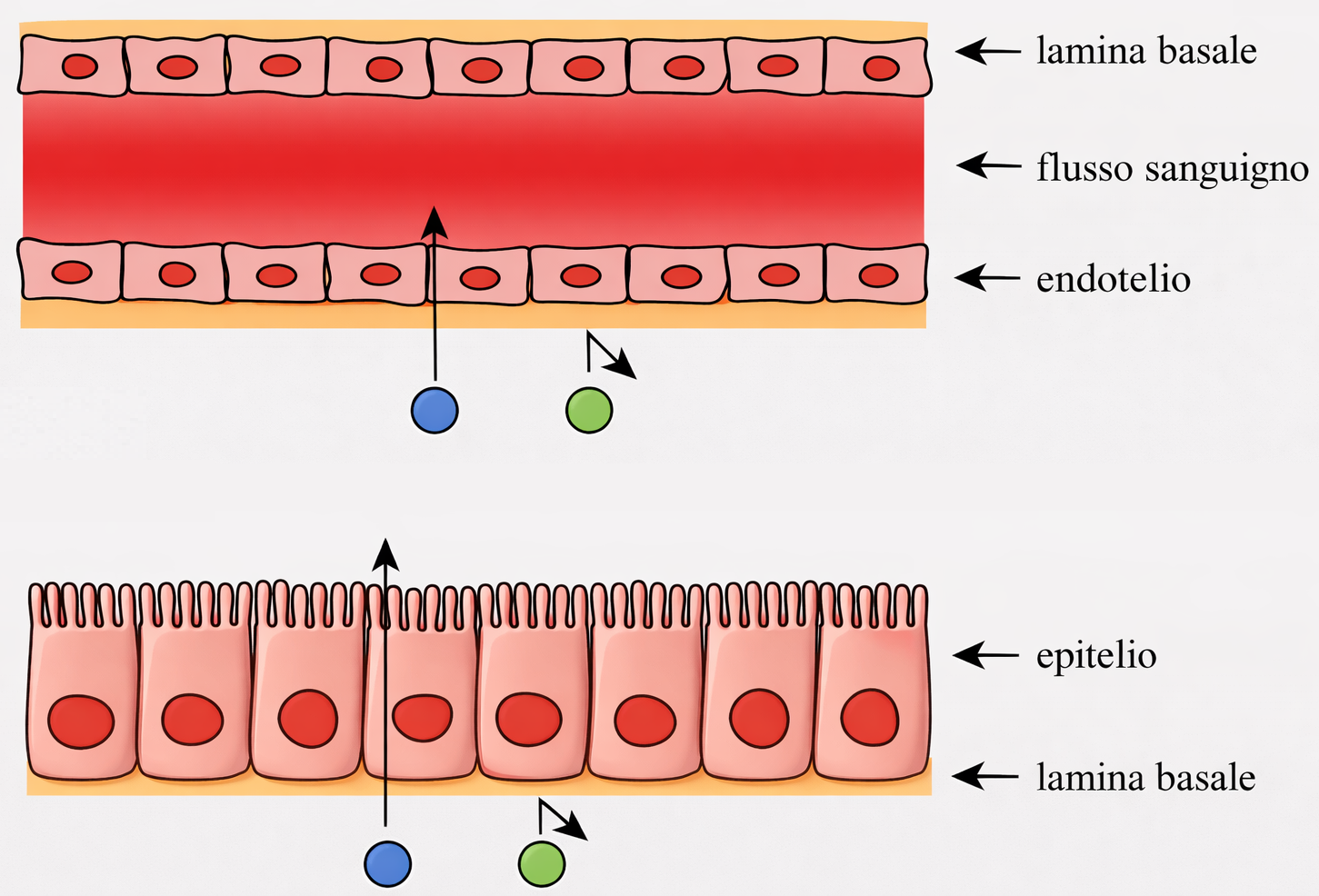
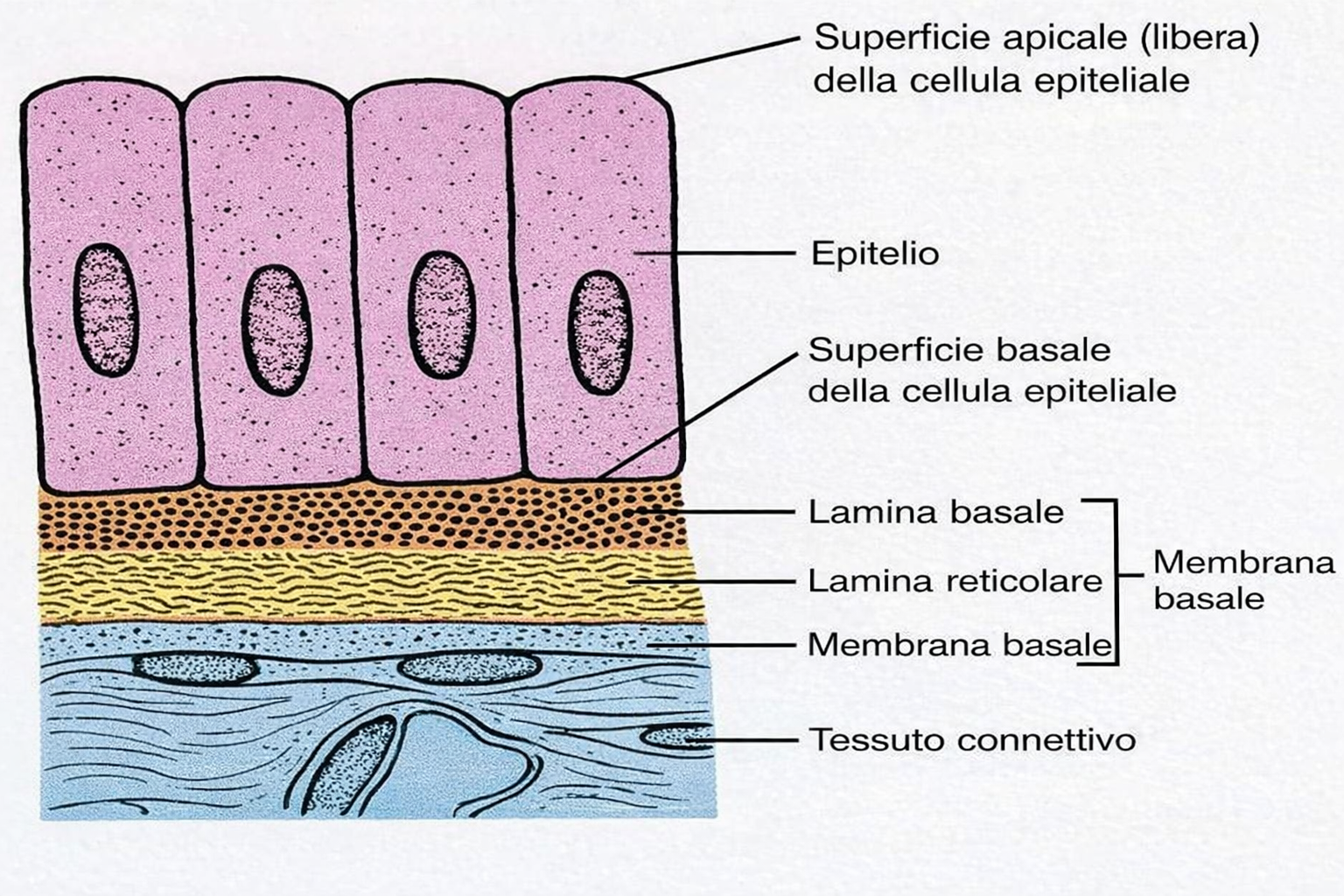
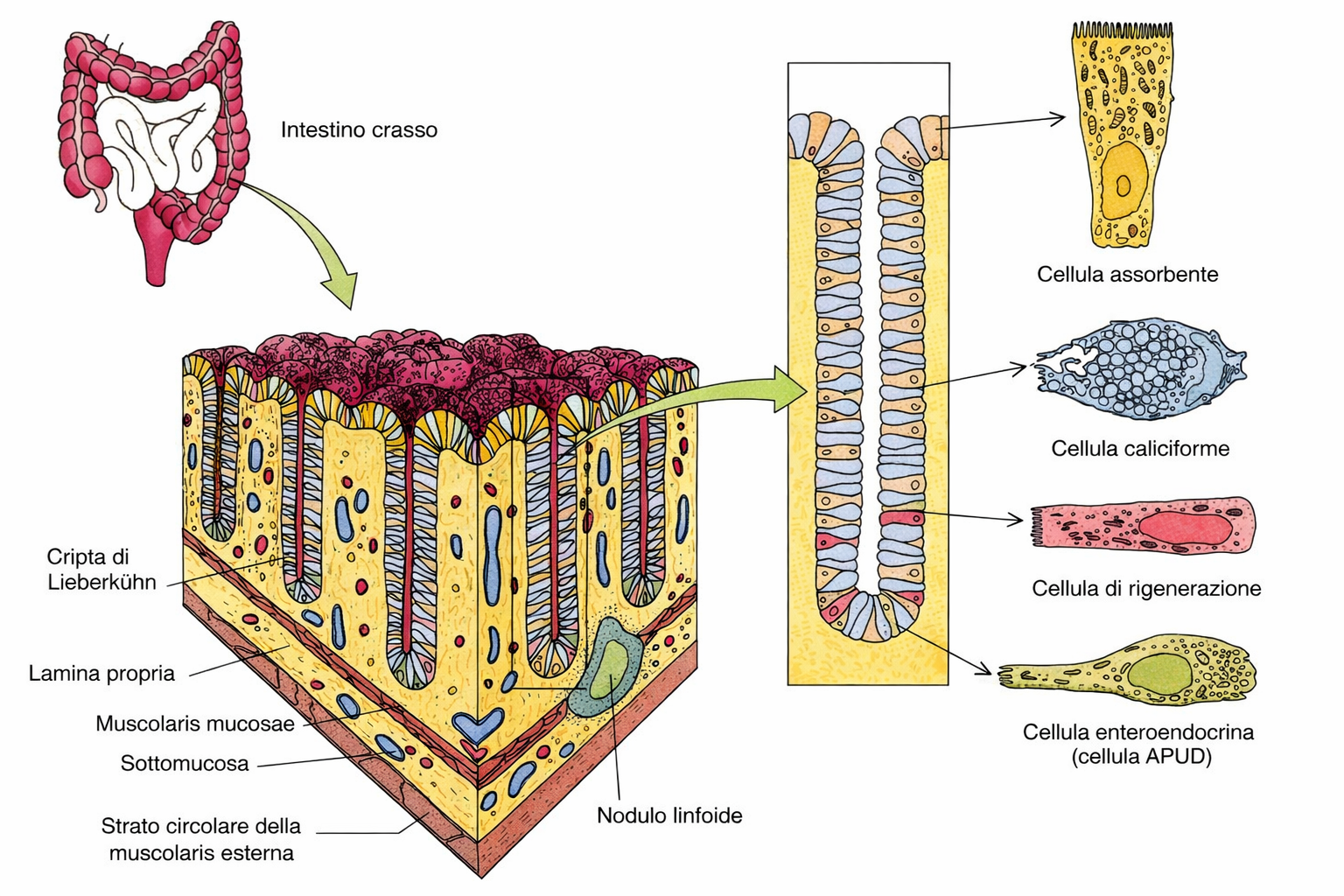
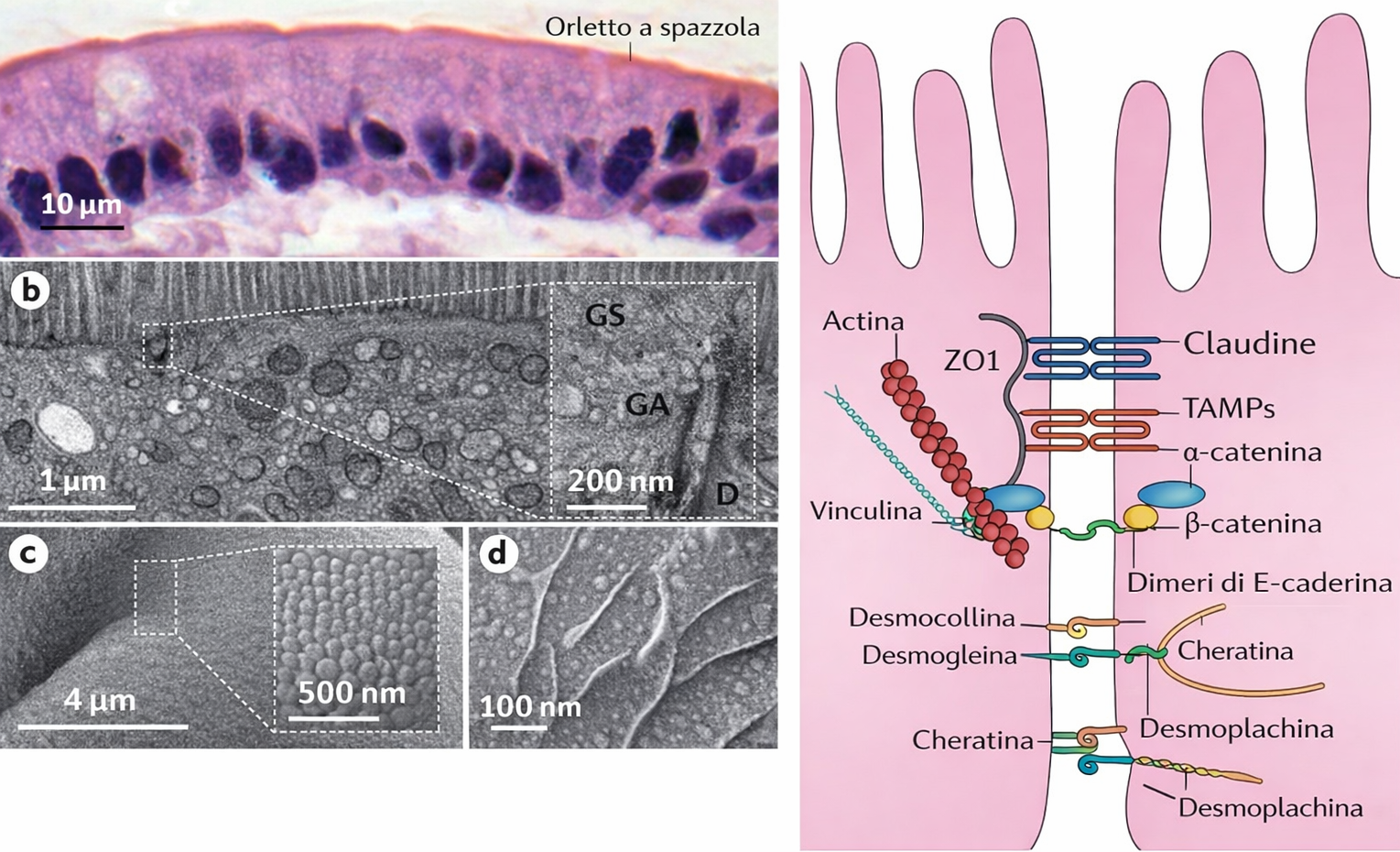
Ogni foglietto epiteliale presenta due facce funzionalmente distinte: la superficie apicale, esposta all’aria o a un lume acquoso, e la superficie basale, in continuità con un sottostante tessuto connettivo attraverso un sottile strato specializzato di matrice extracellulare, la lamina basale (Figura 06.03-02). Tale lamina è costituita principalmente da collagene di tipo IV e da laminina, organizzati in reti macromolecolari che conferiscono resistenza e ancoraggio (Figura 06.03-03). La laminina espone siti di legame per integrine espresse sul versante basale della membrana plasmatica delle cellule epiteliali, fornendo un accoppiamento meccanico e biochimico analogo a quello mediato dalla fibronectina in altri distretti connettivali. In aggiunta, proteine di collegamento come nidogeno/entactina e proteoglicani eparansolfati contribuiscono alla stabilità del reticolo e alle sue proprietà di filtrazione. La polarità apico-basale è un attributo cruciale: domini di membrana distinti ospitano repertori diversi di canali, trasportatori e recettori, coordinando flussi direzionati di sostanze. Nell’epitelio cilindrico semplice dell’intestino tenue, due popolazioni cellulari prevalgono: gli enterociti assorbenti e le cellule caliciformi mucipare (Figura 06.03-04). Gli enterociti internalizzano nutrienti dal lume tramite il dominio apicale, spesso ampliato da un orletto a spazzola di microvilli, e li rilasciano attraverso la membrana basolaterale verso i capillari del connettivo. Per realizzare il trasporto vettoriale, i trasportatori sono segregati in domini: proteine specifiche per l’ingresso apicale e altre, distinte, per l’efflusso basale. Le cellule caliciformi, invece, organizzano l’apparato di Golgi, le vescicole secretorie e il citoscheletro lungo l’asse apico-basale in modo da accumulare e liberare selettivamente mucine dal solo polo apicale (Figura 06.03-04). Il mantenimento di tale asimmetria dipende da:
- interazioni cellula-matrice, mediate da integrine e da specializzazioni come gli emidesmosomi, che collegano i filamenti intermedi alla lamina basale attraverso laminina e collagene di tipo IV;
- giunzioni intercellulari che definiscono barriere laterali e piattaforme di segnalazione;
- complessi di polarità intracellulare (ad esempio Par, Crumbs e Scribble) che, ancorati alla membrana, orchestrano la distribuzione di organelli, il traffico vescicolare e l’architettura del citoscheletro.
Oltre alla funzione di supporto, la lamina basale partecipa alla rigenerazione tissutale come substrato per la migrazione, e in distretti specializzati, come il glomerulo renale, contribuisce alla filtrazione selettiva delle macromolecole.
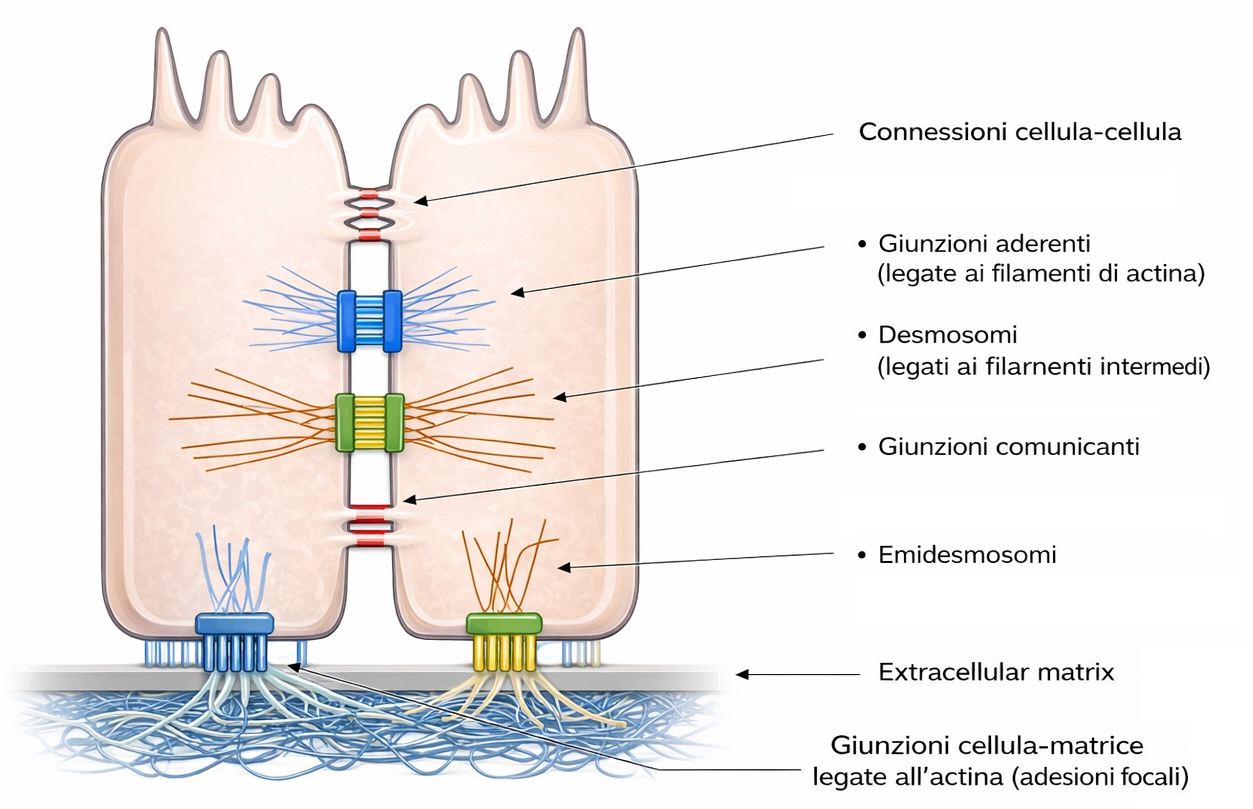
Le connessioni intercellulari degli epiteli si raggruppano per funzione in tre grandi categorie: elementi occludenti che sigillano lo spazio intercellulare, giunzioni di ancoraggio che trasferiscono forze meccaniche tra cellule e matrice, e giunzioni comunicanti che permettono il passaggio di segnali e piccoli soluti. In genere, uno stesso epitelio integra tutti questi moduli in una cintura funzionale continua. Ogni classe risulta dalla combinazione di specifiche proteine transmembrana, adattatori citoplasmatici e collegamenti al citoscheletro. Nei vertebrati, la sigillatura è affidata alle giunzioni strette (tight junctions), che formano un anello continuo alla sommità del compartimento laterale, impedendo il flusso paracellulare di molecole idrofile tra cellule adiacenti. In esperimenti con traccianti, una sostanza applicata dal lato apicale non oltrepassa la giunzione verso il compartimento basolaterale (Figura 06.03-05). A livello molecolare, le tight junctions consistono in filamenti sigillanti composti da claudine e occludina, organizzati in creste anastomizzate allineate lungo la regione di contatto tra membrane contigue (Figura 06.03-05). Adattatori intracitoplasmatici come ZO-1, ZO-2 e ZO-3 connettono questi elementi alla corticale di actina, fungendo da piattaforme per complessi di polarità. Il loro contributo è duplice:
- funzione “gate”: controllano la permeabilità paracellulare in modo tessuto-specifico, con claudine diverse che conferiscono selettività per dimensione e carica, essenziale per il trasporto transepiteliale efficiente;
- funzione “fence”: costituiscono una barriera laterale alla diffusione laterale di proteine e lipidi nel doppio strato, preservando la segregazione tra domini apicali e basolaterali e quindi la polarità funzionale.
Senza la sigillatura, i gradienti generati dal trasporto vettoriale collasserebbero, poiché il percorso paracellulare cortocircuiterebbe il flusso transcellulare. In termini semplificati, il flusso paracellulare di un soluto può essere espresso come \[ J_{para} = P_{para}\,\Delta C, \] dove \(P_{para}\) dipende dall’architettura delle tight junctions e dalla composizione in claudine: epiteli “leaky”, come segmenti prossimali del nefrone, mostrano \(P_{para}\) relativamente elevato, mentre epiteli “tight”, come quello vescicale, presentano \(P_{para}\) molto basso. La capacità delle tight junctions di reclutare complessi Par e di modulare l’organizzazione dell’actina conferisce, inoltre, un controllo diretto sulla definizione dell’apice e della base cellulari. In molti distretti, le giunzioni strette cooperano con giunzioni aderenti, desmosomi ed emidesmosomi per integrare continuità di barriera, integrità meccanica e segnalazione. Questa integrazione garantisce che la parete epiteliale resti coesa, selettiva e capace di risposte adattative a sollecitazioni meccaniche e chimiche variabili.
La coesione meccanica degli epiteli si basa su tre famiglie di giunzioni specializzate, organizzate come complessi transmembrana collegati ai principali sistemi del citoscheletro. Le giunzioni aderenti e i desmosomi assicurano l’adesione cellula–cellula, mentre gli emidesmosomi saldano l’epitelio alla lamina basale. In tutti i casi, proteine di adesione attraversano la membrana e si agganciano, sul versante citoplasmatico, a filamenti di actina o di cheratina. In tal modo, i filamenti citoscheletrici delle cellule adiacenti si interconnettono in una rete continua che distribuisce le forze lungo l’intero foglietto epiteliale.
Le giunzioni aderenti e i desmosomi condividono un principio molecolare: sono costruite attorno a caderine, proteine transmembrana che mediano interazioni omofile, ossia tra molecole dello stesso tipo sulle cellule contigue (Figura 06.03-06). L’affinità di legame delle caderine dipende dagli ioni \( \mathrm{Ca^{2+}} \) extracellulari, che stabilizzano i loro domini extracellulari e conferiscono rigidità al braccio adesivo.
Nelle giunzioni aderenti, tipicamente formate da caderine classiche (ad esempio E-caderina), il dominio citoplasmatico interagisce con un set di adattatori (tra cui catenine, p120-catenina, vinculina, α-actinina, EPLIN) che connettono la giunzione ai fasci di actina corticale. Spesso queste giunzioni si organizzano in una cintura continua (fascia di adesione) a livello sottogiunzionale, appena al di sotto delle giunzioni strette, lungo tutto il perimetro della cellula epiteliale (Figura 06.03-07). Poiché i fasci di actina di cellule vicine risultano allineati e collegati, l’epitelio acquisisce una “maglia” contrattile, regolata da miosina II e da vie a GTPasi Rho, capace di generare tensione e rimodellare la geometria del foglietto.
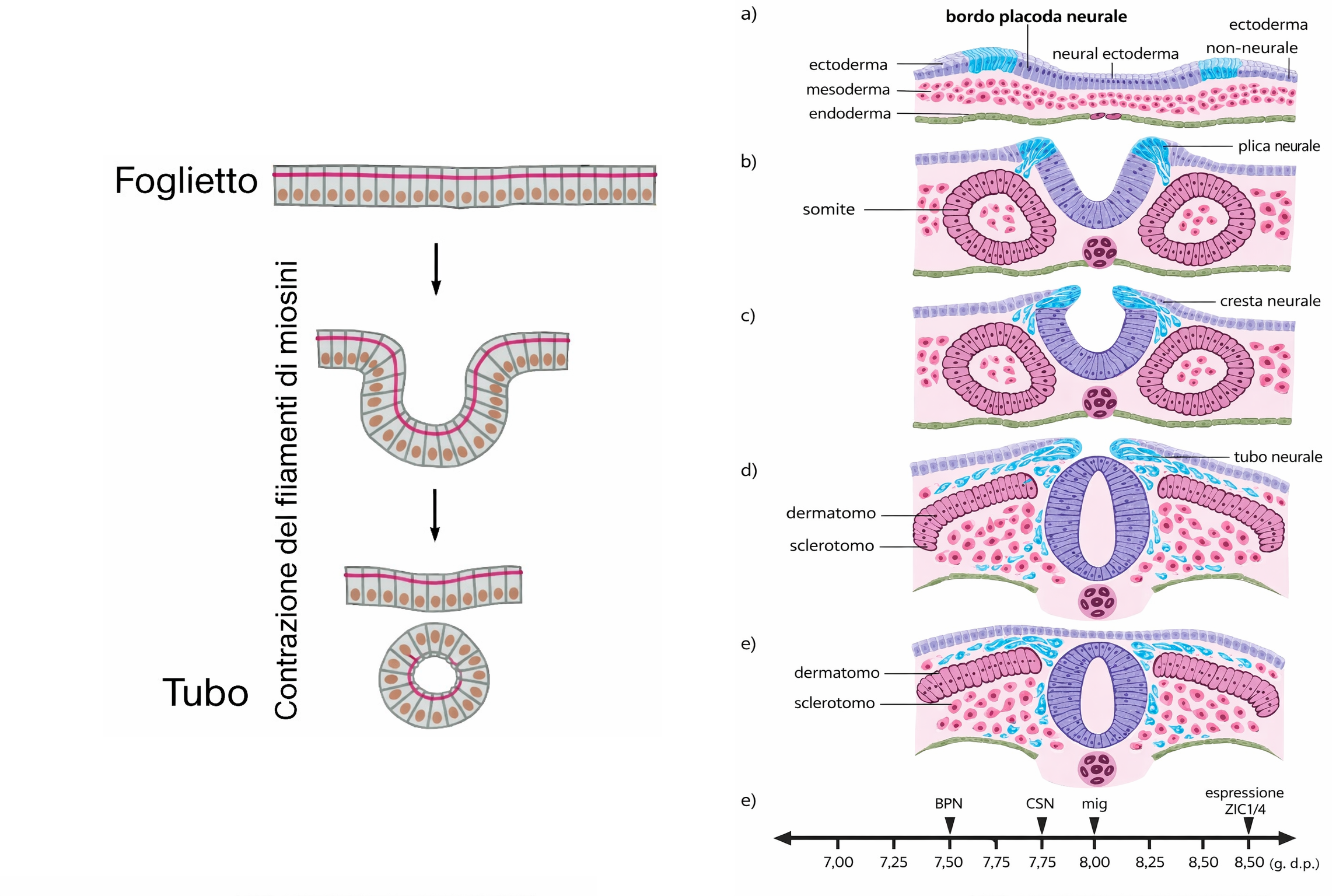
La contrazione coordinata della regione apicale può provocare, a seconda della distribuzione spaziale della tensione, trasformazioni morfogenetiche rilevanti: un restringimento apicale esteso può indurre l’invaginazione e la formazione di strutture tubulari (Figura 06.03-08); una costrizione apicale focale, isotropica e sincrona, può produrre una depressione emisferica che evolve in una vescicola chiusa, separandosi dall’epitelio di origine (Figura 06.03-08). Questi processi sono caratteristici dello sviluppo embrionale, in cui, per esempio, la chiusura del tubo neurale e la genesi della vescicola del cristallino dipendono dall’attività contrattile della cintura di actina ancorata alle giunzioni aderenti.
Nei desmosomi, le caderine sono rappresentate da desmogleine e desmocolline, che si associano a una placca citoplasmatica ricca di desmoplakina, plakoglobina e plakofiline, creando un punto d’ancoraggio robusto per i filamenti intermedi di cheratina. I cordoni di cheratina, così vincolati, attraversano il citoplasma e si connettono, tramite i desmosomi, ai corrispettivi fasci della cellula adiacente (Figura 06.03-09). Questa architettura conferisce all’epitelio un’elevata resistenza a trazione e taglio, caratteristica degli epiteli soggetti a stress meccanici ripetuti, come l’epidermide o l’epitelio della cavità orale.
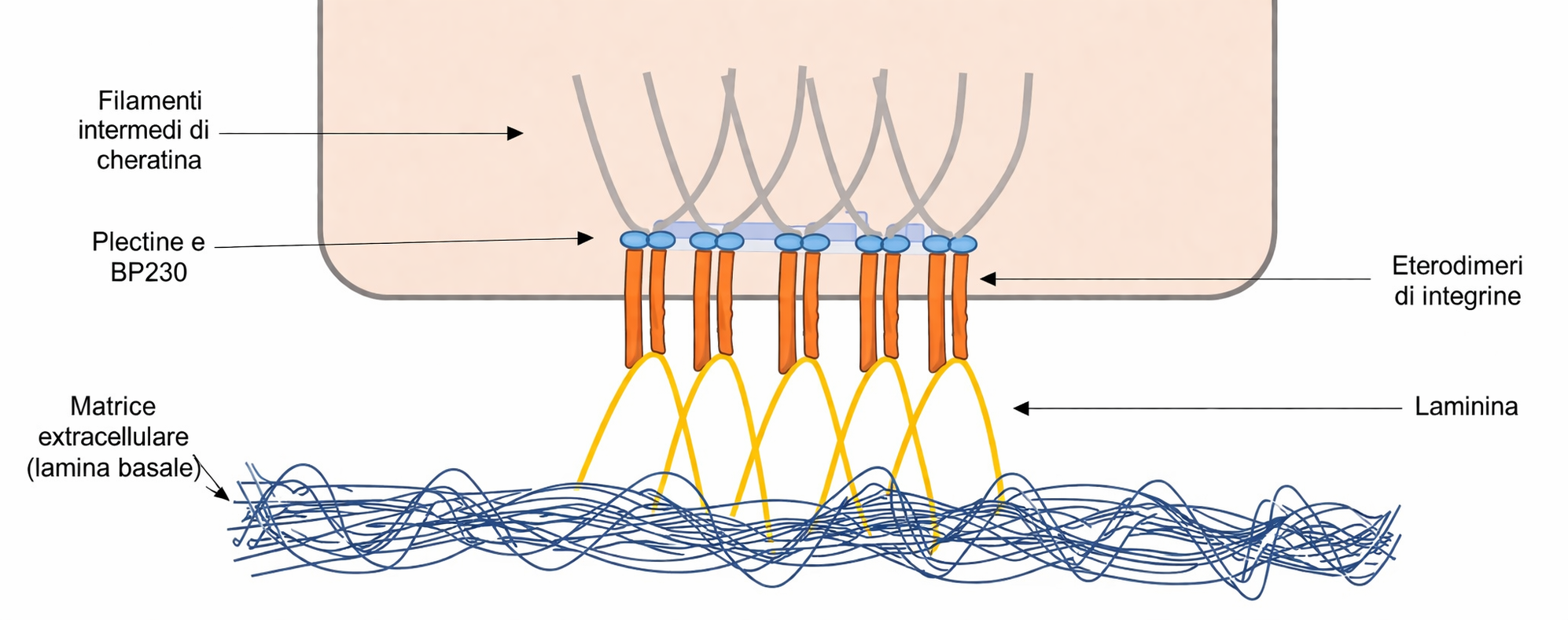
La sola adesione cellula–cellula non basta a impedire il distacco dell’epitelio dal suo letto connettivale: è indispensabile l’ancoraggio alla matrice basale. Questo è affidato alle integrine della membrana basale, in particolare eterodimeri come α6β4, che legano componenti della lamina basale quali la laminina. Sul versante citoplasmatico, le code delle integrine reclutano proteine come plectina e BPAG1e e si collegano ai filamenti di cheratina, configurando strutture che al microscopio ricordano “mezzi desmosomi”, da cui il termine emidesmosomi (Figura 06.03-10). Difetti genetici o autoimmuni di questi complessi producono fragilità del contatto epitelio–matrice e favoriscono la formazione di bolle cutanee:
- giunzioni aderenti: caderine classiche collegate ai fasci di actina; contrazione modulata da miosina II, Rho/ROCK, catenine e vinculina;
- desmosomi: caderine specifiche (desmogleine/desmocolline) ancorate ai filamenti intermedi di cheratina tramite una placca densa contenente desmoplakina e armadilline;
- emidesmosomi: integrine basali (ad esempio α6β4) che legano laminina nella lamina basale e si connettono ai filamenti di cheratina mediante plectina e proteine affini.
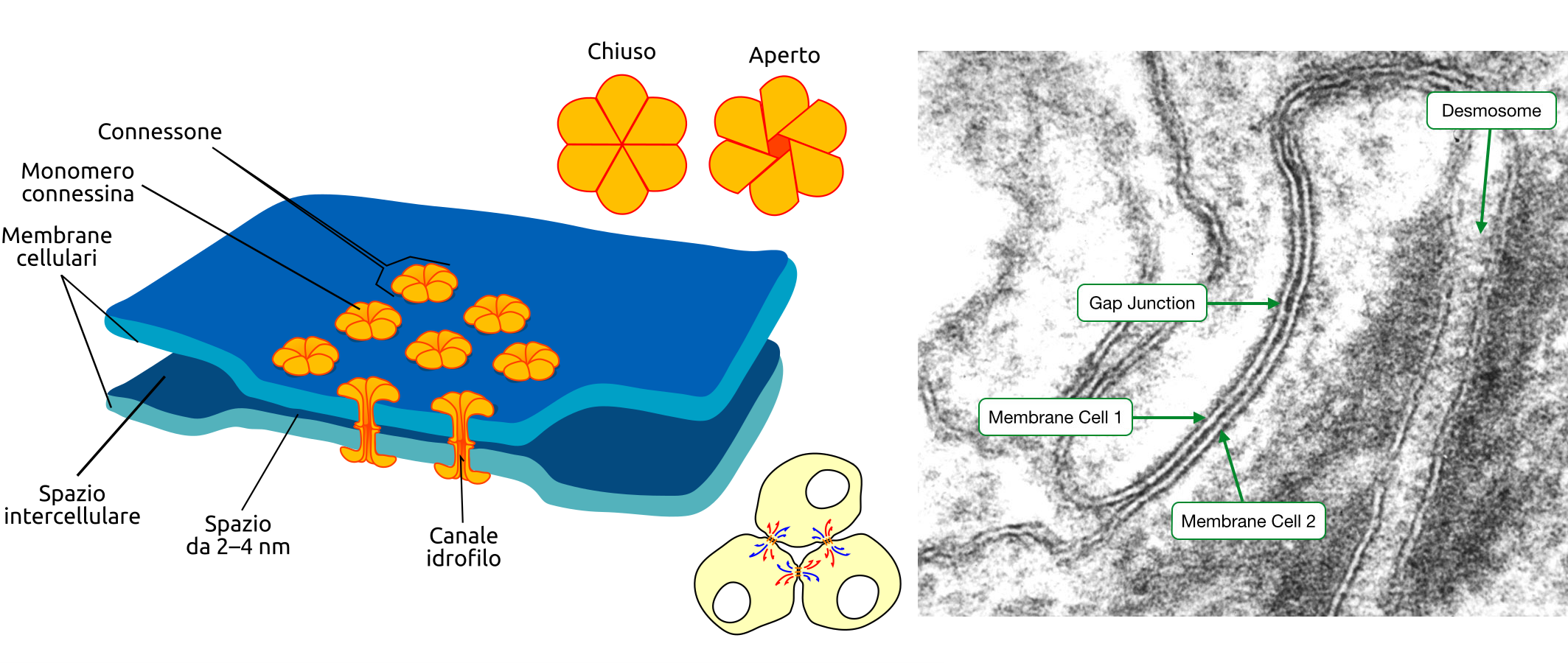
Accanto alle giunzioni di adesione, molti epiteli e numerosi altri tessuti animali possiedono giunzioni comunicanti. Al microscopio elettronico queste appaiono come zone in cui le due membrane plasmatiche si decorrono parallelamente a brevissima distanza (2–4 nm) e sono connesse da complessi proteici simmetrici. Ciascun complesso, detto connessone, è un canale acquoso che nasce dall’allineamento testa a testa di due emicanali omologhi presenti nelle membrane delle cellule adiacenti (Figura 06.03-11). I pori risultanti consentono il passaggio diretto di ioni inorganici e di piccole molecole idrofile, con un limite di massa molecolare di circa \( \leq 1000\,\mathrm{Da} \). Tra i soluti che diffondono figurano secondi messaggeri come \( \mathrm{Ca^{2+}} \), AMP ciclico e \( \mathrm{IP_3} \), creando accoppiamento elettrico e metabolico tra cellule contigue.
Nel miocardio, la presenza di giunzioni comunicanti tra cardiomiociti facilita la propagazione sincronizzata dei potenziali d’azione e coordina la contrazione del tessuto, contribuendo al ritmo cardiaco. Fenomeni analoghi sostengono la contrazione orchestrata della muscolatura liscia e la condivisione di metaboliti tra cellule gliali.
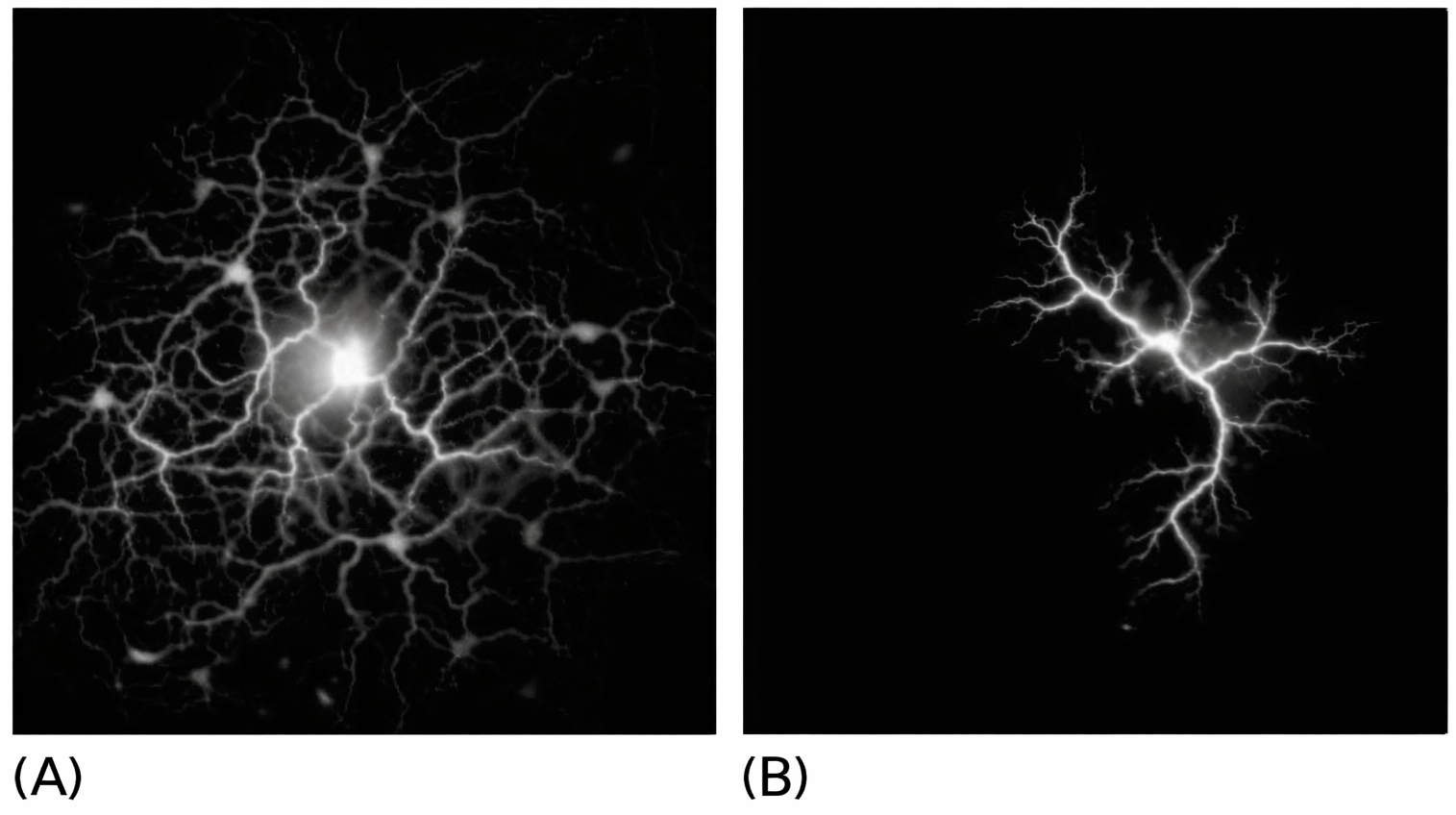
La permeabilità delle giunzioni comunicanti è dinamica e regolata da segnali intra- ed extracellulari. Un esempio emblematico è l’azione della dopamina su specifici circuiti della retina: l’aumento dell’illuminazione induce rilascio di dopamina, che riduce la comunicazione tramite connessoni in una classe di neuroni retinici, ricalibrando la trasmissione elettrica e favorendo il passaggio da un’elaborazione basata sui bastoncelli a una centrata sui coni, ottimizzata per colori e dettagli fini (Figura 06.03-12). Una sintesi delle funzioni delle diverse giunzioni nei tessuti animali:
- stimoli che modulano l’apertura/chiusura: pH citosolico, concentrazione di \( \mathrm{Ca^{2+}} \) intracellulare, differenze di potenziale transgiunzionale, fosforilazione delle connessine da parte di chinasi come PKA/PKC;
- conseguenze fisiologiche: controllo della sincronizzazione elettrica, diffusione di secondi messaggeri, coordinamento metabolico locale.
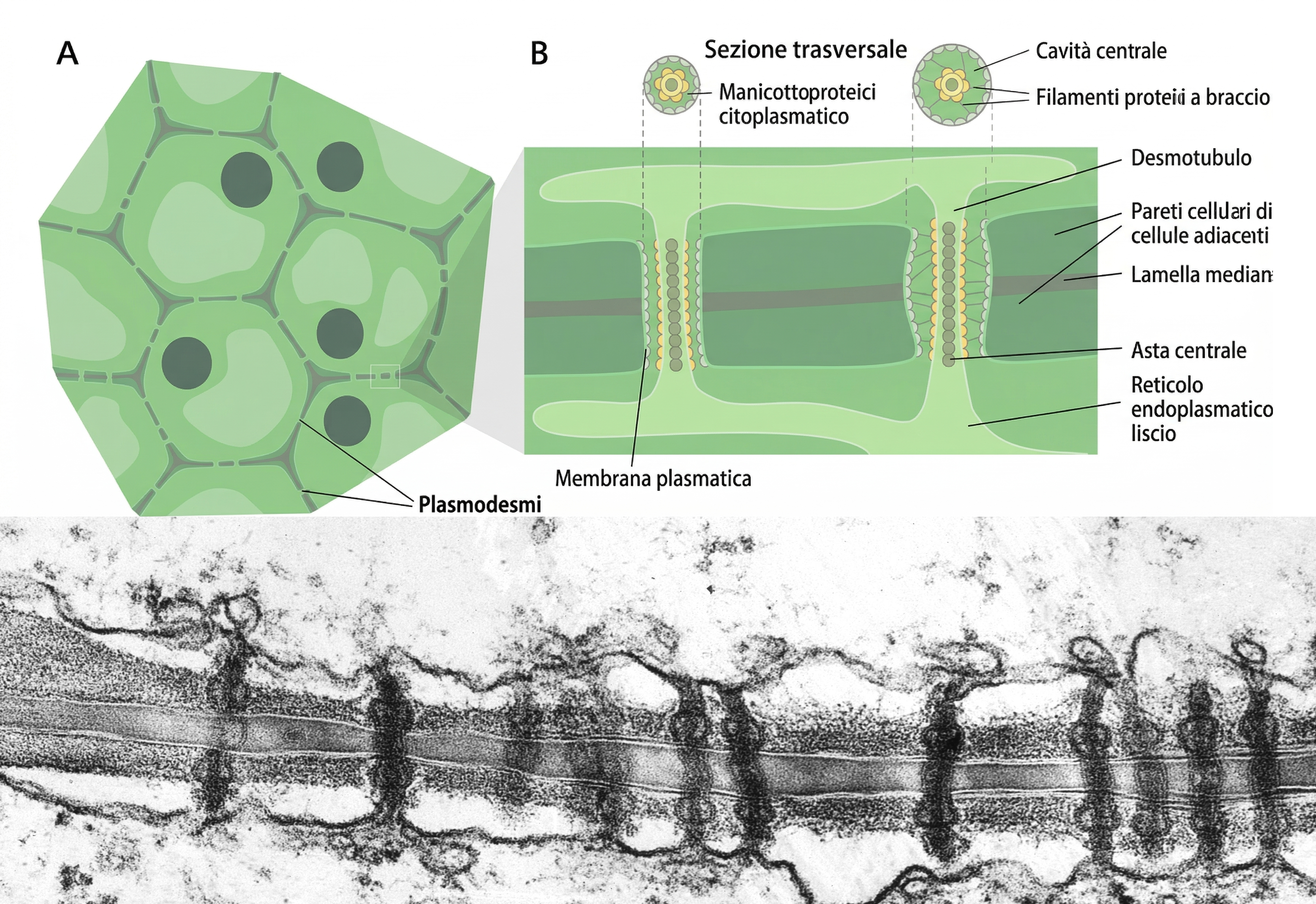
Nei tessuti vegetali mancano le giunzioni descritte per gli animali, poiché l’adesione è mediata dalle pareti cellulari. Esiste però un’analogia funzionale delle giunzioni comunicanti: i plasmodesmi, sottili canali che attraversano la parete e mettono in continuità i citoplasmi di cellule contigue (Figura 06.03-13). A differenza dei connessoni, i plasmodesmi sono rivestiti dalla membrana plasmatica e contengono un desmotubulo, continuità del reticolo endoplasmatico liscio. Questo arrangiamento realizza, in linea teorica, una continuità citoplasmatica cellula–cellula. Oltre a ioni e piccole molecole, possono transitare specifiche macromolecole, tra cui proteine regolative e RNA non codificanti; la regolazione del calibro del poro, anche tramite deposizione di callosio, modula selettivamente il traffico, con un impatto cruciale sui gradienti di fattori regolatori durante lo sviluppo della pianta.